Therapeutisches Ziel: Nierenprotektion
Autor:
OA Dr. Roland Edlinger
3. Medizinische Abteilung für Stoffwechselerkrankungen und Nephrologie
Klinik Hietzing
Karl-Landsteiner-Institut für Stoffwechsel-erkrankungen & Nephrologie, Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Um die Entwicklung einer diabetischen Nierenerkrankung („diabetic kidney disease“; DKD) hintanzuhalten, sind eine frühzeitige und konsequente Blutzucker- und Blutdruckeinstellung wichtige präventive Maßnahmen. Etwa 20–40% aller Menschen mit Typ-2-Diabetes (T2D) entwickeln eine diabetische Nierenerkrankung, die zusammen mit der arteriellen Hypertonie über 50% der Ursachen für eine Nierenersatztherapie ausmacht.
Keypoints
-
Diabetes mellitus und arterielle Hypertonie sind die häufigsten Ursachen einer chronischen Nierenerkrankung und Dialysepflichtigkeit.
-
Optimierte Blutzucker- und Blutdruckeinstellung sowie eine RAS-Blockade ab einer UACR >30mg/g sind die Basis, um eine Progression einer DKD zu verlangsamen.
-
Für SGLT2-Hemmer besteht bei DKD mit einer eGFR >20ml/min/1,73m2 eine 1A-Empfehlung.
-
Bei einer eGFR >25ml/min/1,73m2 und einer UACR >30mg/g besteht für nsMRA eine 2A-Empfehlung (KDIGO 2024).
-
GLP-1-RA stellen nach ADA die 4. Säule in der Nephroprotektion bei DKD dar (Evidenzklasse A, 2025).
Der Entstehung einer Nierenerkrankung kann vor allem bei einem Typ-2-Diabetes oder Bluthochdruck in der Anamnese therapeutisch gut vorgebeugt werden. Als gängige Frühprävention einer diabetischen Nierenerkrankung gilt die bevorzugte Verwendung von Renin-Angiotensin-System-Inhibitoren (RASi) ab einer Albumin-Kreatinin-Ratio im Spontanharn >30mg/g. Darüber hinaus konnten SGLT2-Hemmer (SGLT2i), der nichtsteroidale Mineralokortikoid-Antagonist (nsMRA) Finerenon und Inkretinanaloga spezielle organprotektive Wirkungen auf die Nieren und das kardiovaskuläre System in Studien unter Beweis stellen.
Leitlinien & Studienhintergrund
In den Empfehlungen der amerikanischen Diabetesgesellschaft (ADA) zum Diabetesmanagement und in den KDIGO-Leitlinien zum Management chronischer Nierenerkrankungen 2024 finden GLP-1-Rezeptor-Agonisten (GLP-1-RA) bei T2D und DKD eine positive Empfehlung. Sie sind besonders bei Unverträglichkeit oder Kontraindikation einer SGLT2i-Therapie bzw. bei fehlendem Erreichen des individuellen Glykämiezieles anzuraten. Bis zur Präsentation der FLOW-Studie im Juni 2024 auf dem Kongress der European Renal Association (ERA) in Stockholm war die Empfehlung für GLP-1-RA aus nephroprotektiver Sicht sehr zurückhaltend. Der Grund dafür lag darin, dass in den großen kardiovaskulären Outcomestudien mit Liraglutid, Dulaglutid und Semaglutid Patienten mit DKD nur unzureichend abgebildet waren. Verglichen mit dem Ausgangswert zu Studienbeginn lag die mittlere eGFR deutlich über 60ml/min und es gab keine bzw. nur eine geringe bis mäßiggradige Albuminurie mit einer UACR (Urin-Albumin-Kreatinin-Ratio) <300mg/g. Dass der kombinierte renale Endpunkt in diesen Studien trotzdem positiv war, lag an einem selteneren Auftreten einer De-novo-Albuminurie mit einer UACR >300mg/g.1
In einer gepoolten Analyse der LEADER- und SUSTAIN-6-Studie mit Liraglutid bzw. Semaglutid war der eGFR-Abfall in jener Subgruppe mit einer Ausgangs-eGFR zwischen 30 und 60ml/min signifikant geringer.2 Neben dem deutlich reduzierten primären kombinierten renalen Endpunkt getragen von einer De-novo-Makroalbuminurie (UACR >300mg/g) konnte in einer Sensitivitätsanalyse der REWIND-Studie für Dulaglutid eine signifikante Reduktion von 30% für einen mehr als 40%igen eGFR-Abfall gezeigt werden.3
Eine Metaanalyse aus dem Jahr 2021 bestätigte für GLP-1-RA eine signifikante 21%ige Reduktion des kombinierten renalen Endpunktes, jedoch nur eine nicht signifikante Reduktion von 14% des eGFR-Abfalles.4
Nephroprotektive Mechanismen von GLP-1-Rezeptor-Agonisten
Es werden neben kardiovaskulären und nephroprotektiven Mechanismen von GLP-1-RA durch eine blutzucker-, blutdrucksenkende sowie eine gewichtsreduzierende Wirkung auch antiinflammatorische, natriuretische und antiatherosklerotische Mechanismen diskutiert. Insbesondere das viszerale Fettgewebe scheint bei Adipositas neben einer Aktivierung des Renin-Angiotensin-Systems (RAS) auch durch Freisetzung von Zytokinen maßgeblich an einem nierenschädigenden proinflammatorischen Milieu beteiligt zu sein.5
Die Bedeutung einer persistierenden Gewichtsabnahme durch intensivierte Lebensstilmodifikation konnte erst unlängst in einer Post-hoc-Analyse der Look-AHEAD-Studie bestätigt werden. Eine anhaltende Gewichtsabnahme über einen Zeitraum von 4 Jahren bei einer „time in range“ (TIR) von mindestens 70% hinsichtlich einer zumindest 7%igen Reduktion vom Ausgangsgewicht konnte mit einer Reduktion des kombinierten renalen Endpunktes um 46% in Verbindung gebracht werden (eGFR-Abfall >30% auf unter 60ml/min/1,73m2, eGFR <15ml/min/1,73m2 oder eine Nierenersatztherapie).6
GLP-1-RA konnten in experimentellen Studien zusätzliche antiinflammatorische, antioxidative und antifibrotische sowie auch vasodilatierende Effekte zeigen. Der Mechanismus dürfte vor allem auf dem von viszeralen Adipozyten freigesetzten Muster an Zytokinen und Adipokinen und auf dem Einfluss auf die ektope Fettakkumulation beruhen.7–9 Ein weiterer potenzieller Mechanismus wurde erst rezent beschrieben. Experimentell fand sich bei Mäusen, bei denen der GLP-1-Rezeptor ausgeschaltet wurde (GLP-1-Knock-out), eine Zunahme der Albuminurie, die durch den zusätzlichen Diabetesstatus noch verstärkt wird. Gleichzeitig zeigte sich auch eine Hochregulation des Rezeptors für „Advanced Glycation End Products“ (RAGE). Dieselbe RAGE-Hochregulation war auch bei nicht diabetischen albuminurischen Versuchstieren nach subtotaler Nephrektomie mit glomerulärer Hyperfiltration zu beobachten. Eine Co-Deletion des RAGE reduzierte den Effekt des GLP-1-Knock-outs auf die Albuminurie.
Durch Liraglutid konnten sowohl die RAGE-Expression im renalen Kortex als auch die Albuminurie reduziert werden, sodass eine pathophysiologische Bedeutung des RAGE bei der podozytären Schädigung zu postulieren wäre, die durch einen GLP-1-RA zumindest teilweise hintangehalten werden kann.10
Weitere Einblicke in die Wirkmechanismen von Semaglutid auf die Niere werden von der laufenden REMODEL-Studie erwartet. Mittels spezieller MRT-Technik sollen wiederholt Nierenperfusion, Oxygenierung, Inflammation und Fibrose in unterschiedlichen Nierenregionen beurteilt werden, außerdem werden in Nierenbiopsiepräparaten Genexpressionsmuster in verschiedenen Zelltypen im Zeitverlauf untersucht.
FLOW-Studie
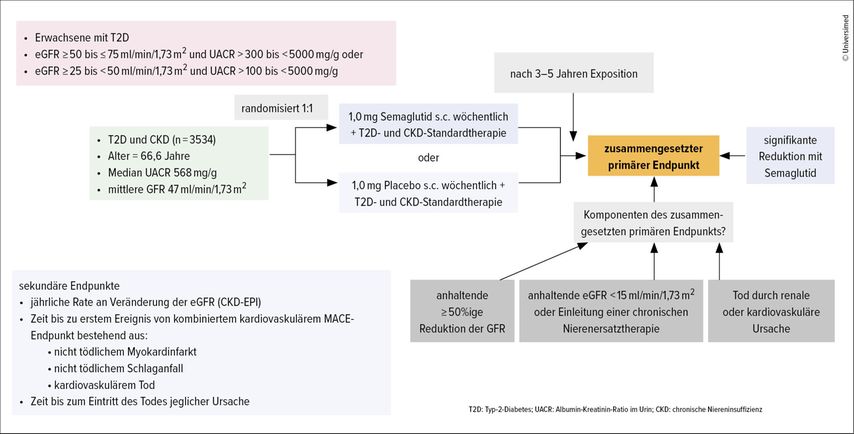
Neben diesen experimentellen Daten und der erwähnten Reduktion kombinierter renaler Endpunkte in den kardiovaskulären Outcomestudien zu GLP-1-RA bestätigte sich für Semaglutid in der rezent publizierten FLOW-Studie die nephroprotektive Wirkung bei Patienten mit manifester bereits fortgeschrittener DKD eindrucksvoll. Im Unterschied zu den kardiovaskulären Outcomestudien waren nach den KDIGO-Kriterien 93% der Patienten mit hohem und sehr hohem Risiko inkludiert.1 Die mittlere eGFR lag bei 47ml/min/1,73m2 und die mittlere UACR bei 568mg/g (Abb. 1).11, 12
Abb. 1: Übersicht über die FLOW-Studie auf einen Blick (nach Rossing P et al. 2023 und Trevella P et al. 2024)11, 12
3533 Studienteilnehmer wurden doppelblind in eine Placebo- und eine Semaglutid-Gruppe randomisiert und über einen medianen Beobachtungszeitraum von 3,4 Jahren untersucht. Der primäre kombinierte renale Endpunkt, bestehend aus einem eGFR-Abfall über 50%, einer eGFR unter 15ml/min/1,73m2 oder Nierenersatztherapie sowie aus dem Tod aus kardiovaskulärer oder renaler Ursache, war signifikant um relative 24% und absolut von 23,2% auf 18,7% reduziert, entsprechend einer NNT („number needed to treat“) von 20 (Woche 156).13 Auch sämtliche sekundäre Endpunkte wurden statistisch signifikant vermindert. Die NNT, um ein kardiovaskuläres Ereignis zu verhindern (MACE: Tod, nicht tödlicher Schlaganfall, nicht tödlicher Myokardinfarkt), lag bei 45 und jene für die Gesamtmortalität bei 39.
In der SELECT-Studie konnte bei über 17000 Patienten mit Adipositas (mittlerer BMI 33) und kardiovaskulärer Erkrankung, jedoch ohne Diabetes der kombinierte renale Endpunkt um 22% reduziert werden. Bei einer mittleren Ausgangs-eGFR von 82ml/min/1,73m2 und großteils Normoalbuminurie und somit geringerem Ausgangsrisiko lag die NNT allerdings mit 250 deutlich höher.14
Nephroprotektion durch Tirzepatid
Auch für den dualen GLP-1- und GIP-Agonisten Tirzepatid existieren Hinweise auf eine nephroprotektive Wirkung. Dies konnte sowohl in einer Post-hoc-Analyse der SURPASS-4-Studie im Vergleich mit Insulin Glargin als auch in einer retrospektiven Kohortenuntersuchung an knapp 15000 Patienten gezeigt werden. In Letzterer hatten höhere Dosen von Tirzepatid einen größeren Effekt.15,16 Allerdings wurden auch hier vorwiegend Patienten mit erhaltener Nierenfunktion und Normoalbuminurie untersucht. Studienergebnisse bei fortgeschrittener DKD fehlen bis dato noch.
Nephroprotektive Kombinationstherapien: GLP-1-RA mit/ohne SGLT2i
Da SGLT2i in den rezenten KDIGO-Empfehlungen bei DKD mit einer eGFR über 20ml/min/1,73m2 einen hohen Empfehlungsgrad mit sehr hohem Evidenzniveau haben (1A), stellt sich klinisch die Frage, welche der beiden Substanzklassen das größere nephroprotektive Schutzpotenzial hat bzw. inwieweit eine Kombination von SGLT2i und GLP-1-RA sinnvoll ist.
Direkte Vergleichsstudien zwischen SGLT2i und GLP-1-RA hinsichtlich des Effekts auf renale Endpunkte existieren nicht, zwei retrospektive Kohortenuntersuchungen an insgesamt ca. 35000 Patienten mit DKD legen eine stärkere nephroprotektive Wirkung von SGLT2i im Vergleich zu GLP-1-RA nahe.17,18
Praxistipp
GLP-1-Rezeptor-Agonisten haben neben blutzuckersenkenden, gewichtsreduzierenden und kardiovaskulär protektiven Wirkungen auch hinsichtlich Nierenschutz einen hohen Stellenwert.In der FLOW-Studie war für Semaglutid ein konsistenter Benefit mit und ohne etablierte SGLT2i-Therapie nachweisbar.19 Auch scheint der zusätzliche Vorteil laut einer britischen Kohortenstudie unabhängig davon zu sein, ob mit einem SGLT2i oder einem GLP-1-RA zuerst begonnen wird.20 In den rezentesten ADA-Empfehlungen vom Jänner 2025 werden bei DKD GLP-1-RA erstmals den SGLT2i gleichgestellt, wobei für beide Substanzklassen das höchste Evidenzniveau der Klasse A angegeben wird.
In Zukunft wird sich in Bezug auf die beiden Substanzklassen allerdings weniger die Frage stellen, SGLT2i oder GLP-1-RA, vielmehr stellt sich die Frage, ob SGLT2i und GLP-1-RA! Eine rezente Datenanalyse der großen Studien bei DKD mit SGLT2i, GLP-1-TA und dem nsMRA Finerenon unterstreicht einen additiven Effekt auf die CKD-Progression, Herzinsuffizienz-Hospitalisierung, MACE sowie die kardiovaskuläre und Gesamtmortalität.21
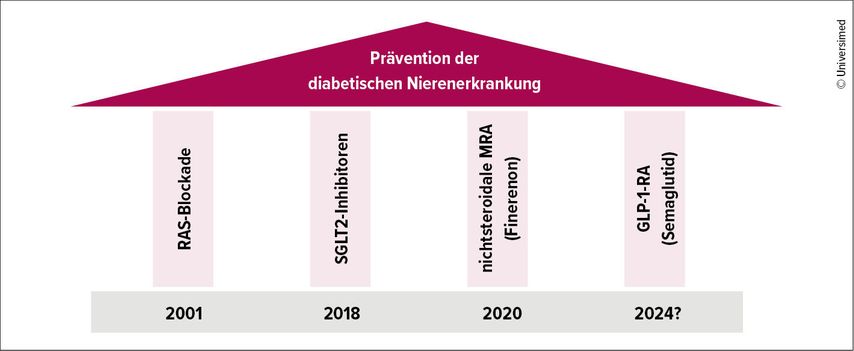
Neben RAS-Blockern, SGLT2-Hemmern und nsMRA werden GLP-1-RA heute auch als die 4. Säule der Nephroprotektion bei DKD bezeichnet (Abb. 2).5,22
Abb. 2: 4 Säulen der pharmakologischen Interventionen, um den Progress einer diabetischen Nephropathie zu verhindern (nach Naaman SC, Bakris GL 2023)5
Literatur:
1 MacIsaac RJ et al.: Glucagon-like peptide-1-receptor agonists and kidney outcomes. J Diabetes 2024; 16(10): e13609 2 Shaman AM et al.: Effect of the glucagon-like peptide-1 receptor agonists semaglutide and liraglutide on kidney outcomes in patients with type 2 diabetes: pooled analysis of SUSTAIN-6 and LEADER. Circulation 2022; 145(8): 575-85 3 Gerstein HC et al.: Dulaglutide and renal outcomes in type 2 diabetes: an exploratory analysis of the REWIND randomised, placebo-controlled trial. Lancet 2019; 394(10193): 131-8 4 Sattar N et al.: Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with type 2 diabetes: a systematic review and meta-analysis of randomised trials. Lancet Diabetes Endocrinol 2021; 9(10): 653-62 5 Naaman SC, Bakris GL: Diabetic nephropathy: update on pillars of therapy slowing progression. Diabetes Care 2023; 46(9): 1574-86 6 Zu C et al.: Association of body weight time in target range with the risk of kidney outcomes in patients with overweight/obesity and type 2 diabetes mellitus. Diabetes Care 2024; 47(3): 371-8 7 Dandona P et al.: Incretins: beyond type 2 diabetes. Diabetes Obes Metab 2018; 20(1): 59-67 8 Jiang Zet al.: Obesity and chronic kidney disease. Am J Physiol Endocrinol Metab 2023; 324(1): 24-41 9 Rroji M, Spasovski G: Transforming diabetes care: the molecular pathways through which GLP1-RA impact the kidneys in diabetic kidney disease. Biomedicines 2024; 12(3): 657 10 Sourris KC et al.: Glucagon-like peptide-1 receptor signaling modifies the extent of diabetic kidney disease through dampening the receptor for advanced glycation end products-induced inflammation. Kidney Int 2024; 105(1): 132-49 11 Rossing P et al.: The rationale, design and baseline data of FLOW, a kidney outcomes trial with once-weekly semaglutide in people with type 2 diabetes and chronic kidney disease. Nephrol Dial Transplant 2023; 38(9): 2041-51 12 Trevella P et al.: Potential kidney protective effects of glucagon-like peptide-1 receptor agonists. Nephrology (Carlton) 2024; 29(8): 457-69 13 Perkovic V et al.: Effects of semaglutide on chronic kidney disease in patients with type 2 diabetes. N Engl J Med 2024; 391(2): 109-21 14 Colhoun HM et al.: Long-term kidney outcomes of semaglutide in obesity and cardiovascular disease in the SELECT trial. Nat Med 2024; 30(7): 2058-66 15 Bosch C et al.: Tirzepatide and prevention of chronic kidney disease. Clin Kidney J 2023; 16(5): 797-808 16 Chuang MH et al.: Clinical outcomes of tirzepatide or GLP-1 receptor agonists in individuals with type 2 diabetes. JAMA Netw Open 2024; 7(8): e2427258 17 Fadini GP et al.: Comparative renal outcomes of matched cohorts of patients with type 2 diabetes receiving SGLT2 inhibitors or GLP-1 receptor agonists under routine care. Diabetologia 2024: 67(11): 2585-97 18 Morello CM et al.: SGLT-2 inhibitors versus GLP-1 receptor agonists effects on kidney and clinical outcomes in veterans with type 2 diabetes. Kidney360 2024; 5(11): 1633-43 19 Mann JFE et al.: Effects of semaglutide with and without concomitant SGLT2 inhibitor use in participants with type 2 diabetes and chronic kidney disease in the FLOW trial. Nat Med 2024; 30(10): 2849-56 20 Simms-Williams N et al.: Effect of combination treatment with glucagon-like peptide-1 receptor agonists and sodium-glucose cotransporter-2 inhibitors on incidence of cardiovascular and serious renal events: population based cohort study. BMJ 2024; 385: e078242 21 Neuen BL et al.: Estimated lifetime cardiovascular, kidney, and mortality benefits of combination treatment with SGLT2 inhibitors, GLP-1 receptor agonists, and nonsteroidal MRA compared with conventional care in patients with type 2 diabetes and albuminuria. Circulation 2024; 149(6): 450-62 22 Agarwal R, Fouque D: The foundation and the four pillars of treatment for cardiorenal protection in people with chronic kidney disease and type 2 diabetes. Nephrol Dial Transplant 2023; 38(2): 253-7
Das könnte Sie auch interessieren:
Neue Daten aus dem VERTIS-Studienprogramm
Die kardiovaskuläre Sicherheitsstudie VERTIS CV mit dem SGLT2-Inhibitor Ertugliflozin verlief weniger günstig als andere Endpunktstudien zu dieser Substanzgruppe. Die Hintergründe dafür ...
Liraglutid - Hoffnung auf Betazellprotektion
Mit der Kombination eines Immunmodulators mit dem GLP-1-Analogon Liraglutid konnte in einer Population von Patienten mit neu diagnostiziertem Typ-1-Diabetes der Verlust an Betazellen ...
DAPA-CKD: Dapagliflozin schützt die Nieren und reduziert die Mortalität
Im Rahmen des EASD-Kongresses wurden erfreuliche Daten zur Nephroprotektion des SGLT2-Inhibitors Dapagliflozin präsentiert. Dieser reduzierte in der Studie DAPA-CKD in einer Population ...