Inflammation als therapeutischer Angriffspunkt bei Atherosklerose
Autoren:
Dr. Thomas Rathner
Assoz. Prof. Priv.-Doz. Dr. Heiko Bugger
Klinische Abteilung für Kardiologie, Medizinische Universität Graz
E-Mail: heiko.bugger@medunigraz.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Atherosklerose ist die Hauptursache kardiovaskulärer Erkrankungen, die weiterhin die häufigste Todesursache in Industrienationen darstellen. Eine chronische Entzündung der Gefäßwand verursacht und verstärkt die atherosklerotische Plaqueentwicklung, die durch antiinflammatorische Therapie ausgebremst werden kann. Daher ist nun zur optimalen Einstellung der kardiovaskulären Risikofaktoren und Senkung der Ereignisrate bei Menschen mit chronischem Koronarsyndrom eine zusätzliche Therapie mittels Colchicin seitens der European Society of Cardiology (ESC) empfohlen.
Keypoints
-
Atherosklerose der Herzkranzgefäße ist eine inflammatorische Erkrankung.
-
Spezifische antiinflammatorische Therapie kann kardiovaskuläre Ereignisraten senken.
-
„Low-dose“-Colchicin-Therapie sollte bei Patient:innen mit chronischem Koronarsyndrom (ESC-Klasse-IIa-Empfehlung) unabhängig von hsCRP erwogen werden.
Im Rahmen der Atherosklerose kommt es zur Bildung von sog. atherosklerotischen Plaques in der subintimalen Gefäßwand. Im Koronarsystem können hieraus fluss-limitierende Koronarstenosen entstehen, die das Korrelat eines chronischen Koronarsyndroms mit belastungsabhängiger Angina pectoris darstellen. Atherosklerotische Plaques, insbesondere sog. vulnerable Plaques mit dünner fibröser Kappe, hohem Lipidanteil oder ausgeprägter Entzündung, können jedoch nicht nur gefäßverengend wirken, sondern zeigen auch eine vermehrte Tendenz, zu rupturieren und somit durch akute Thrombosierung des Koronargefäßes einen akuten Herzinfarkt zu verursachen. Insofern sind Pathogenese und Komposition atherosklerotischer Plaques mitentscheidend für das Risiko für klinische Ereignisse.
Inflammation als Antrieb der Entstehung von Atherosklerose
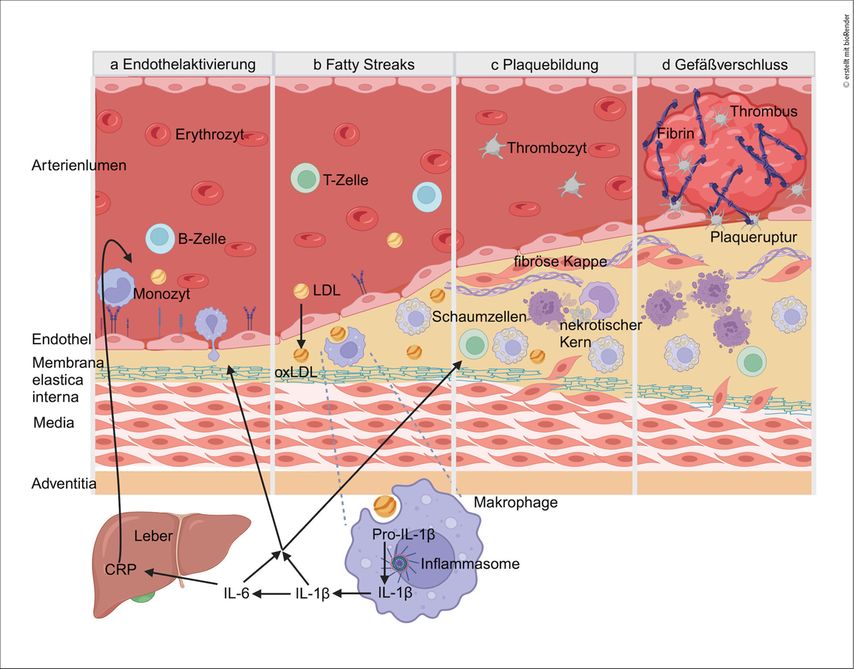
Die Plaqueentstehung startet mit der Schädigung und Aktivierung des gefäßauskleidenden Endothels. Es kommt zu einer Störung der Barrierefunktion sowie zur Rekrutierung von Immunzellen aus der Zirkulation (Abb.1a). „Low density lipoprotein“ (LDL)-Cholesterin akkumuliert in der Folge in der Gefäßwand und es entstehen sog. „fatty streaks“. Die Aktivität der angelockten Entzündungszellen sorgt für freie Radikale, die das Cholesterin oxidieren. In weiterer Folge wird das oxidierte Cholesterin (oxLDL) von Makrophagen aufgenommen, die sich zu Schaumzellen umwandeln. Das oxLDL aktiviert das sog. NLRP3-Inflammasom in den Makrophagen und damit eine vermehrte Ausschüttung von Zytokinen, insbesondere von Interleukin 1 beta (IL-1β) und Interleukin 6 (IL-6) (Abb.1b). Durch den Zelltod der Schaumzellen kommt es innerhalb der wachsenden Plaque schließlich zur Entstehung eines nekrotischen Kerns. Zusätzlich wandern glatte Muskelzellen in die Plaque ein und bilden die bindegewebige fibröse Kappe, die den thrombogenen nekrotischen Kern vom Blutstrom trennt(Abb.1c).1
Abb. 1: Entstehung von Atherosklerose. a: Endothelaktivierung: Aktivierung des Endothels führt zur Transmigration von Leukozyten. b: „fatty streaks“: Durch Akkumulation von LDL-Cholesterin kommt es zur Bildung von „fatty streaks“. Oxidiertes LDL aktiviert das Inflammasom in Makrophagen und IL-1β und IL-6 werden freigesetzt. IL-6 regt die CRP-Produktion in der Leber an. c: Plaquebildung: Makrophagen nehmen oxidiertes LDL (oxLDL) auf und werden zu Schaumzellen. Durch den Zelltod kommt es zur Bildung des nekrotischen Kerns. d: Gefäßverschluss: Die fibröse Kappe reißt auf, es kommt zur Thrombusbildung mit Gefäßverschluss
Aktuelle Studien zeigen jedoch, dass das bisherige Verständnis der menschlichen Atherosklerose als primär von Makrophagen angetriebene Erkrankung überholt ist und tatsächlich T-Zellen häufiger als Makrophagen in der Plaque vorkommen.2 Bemerkenswerterweise findet das Plaquewachstum schubweise statt, wobei das erworbene Immunsystem eine zentrale Rolle spielt. Antigene, insbesondere Apolipoprotein B-100 (ApoB) als wichtigstes Protein in LDL-Partikeln, werden durch antigenpräsentierende Zellen an T-Zellen präsentiert. Im Verlauf schaffen T-Zellen es nicht mehr, Toleranz zu vermitteln, sondern proliferieren und verstärken die Entzündung in der Plaque.1,3 Letztlich werden innerhalb der Plaque zunehmend Enzyme gebildet, die die fibröse Kappe angreifen und ausdünnen. Es kommt durch eine Ruptur der Plaque zu einem Kontakt des Blutstroms mit dem nekrotischen Kern (Abb.1d). Dies induziert eine rasche Thrombusbildung, einen Gefäßverschluss, und kann somit z.B. in dem klinischen Bild eines akuten Koronarsyndroms (ACS) resultieren.
Mittlerweile ist auch bekannt, dass bis zu einem Drittel aller akuten Koronarsyndrome nicht auf einer Ruptur, sondern lediglich auf einer Plaqueerosion beruhen.4 Hierbei führt Stress, der durch Scherkräfte der Zellen an der Gefäßwand entsteht, zu Funktionsstörungen und zum Zelluntergang im Endothel. Im Verlauf kommt es zur Ausbildung von Netzwerken extrazellulärer Fasern (sog. „neutrophil extracellular traps“) und schließlich zu einer Thrombosierung im Gefäß, wobei die strukturelle Integrität der Gefäßwand erhalten bleibt.4 Interessanterweise zeigen sich in Plaques mit Endothelerosion geringere Lipidablagerungen und höhere fibrotische Anteile. Zusätzlich weisen sie weniger Entzündungsaktivität und weniger stenosierendes Wachstum als klassische Plaques auf.4
Entzündungshemmende Therapien reduzieren kardiovaskuläres Risiko
Jede persistierende Entzündung im Körper scheint die vaskuläre Inflammation und somit auch Progression einer Atherosklerose und kardiovaskuläre Ereignisse zu begünstigen.5 Von zentraler Bedeutung ist, dass neben neuen Risikofaktoren, wie viszeraler Adipositas oder Erkrankungen mit bekannter systemischer Inflammation (z.B. rheumatoider Arthritis), auch traditionelle kardiovaskuläre Risikofaktoren (Bluthochdruck, hohes LDL-Cholesterin, Rauchen, Diabetes mellitus) zu einer systemischen Inflammation führen. Tatsächlich reflektiert bereits ein erhöhtes hochsensitives CRP (hsCRP) das residuelle inflammatorische Risiko von kardiovaskulären Risikopatient:innen und kann kardiovaskuläre Ereignisse unabhängig vom LDL-Cholesterin vorhersagen. Die optimale Einstellung der traditionellen Risikofaktoren ist daher besonders wichtig, da hierdurch auch günstige Effekte auf die vaskuläre Inflammation im Rahmen der Atherosklerose bewirkt werden können.6–8
Neben dieser indirekten antiinflam-matorischen Wirkkomponente wurden in den vergangenen Jahren mehrere spezifischere antiinflammatorische Therapien in klinischen Endpunktstudien untersucht. In der CANTOS-Studie wurde an über 10000 Patient:innen mit Myokardinfarkt in der Vorgeschichte und erhöhtem hsCRP der Einfluss von Canakinumab, einem monoklonalen Antikörper gegen IL-1β, auf harte kardiovaskuläre Endpunkte untersucht. Im Vergleich zu Placebo reduzierte die Therapie mit Canakinumab den primären Endpunkt aus Myokardinfarkt, nicht tödlichem Insult und kardiovaskulärem Tod um ca. 15%.9 Bemerkenswerterweise zeigten Analysen, dass jene Patient:innen, bei denen sich das hsCRP nach der ersten Dosis normalisierte, sogar von einer ca. 30%igen Reduktion der Mortalität profitierten.10 Diese Studie zeigt somit, dass Atherosklerose eine inflammatorische Erkrankung ist und antiinflammatorische Therapien tatsächlich klinische Ereignisse reduzieren können. In der Canakinumab-Gruppe kam es zu einem statistisch signifikanten Anstieg tödlicher Infektionen, der jedoch in Anbetracht der hohen Gesamtzahl eingeschlossener Patient:innen als gering eingestuft wurde (23 vs. 29 Patient:innen).9 Bei außerdem ausgeprägt positivem Effekt auf Krebserkrankungen als Nebenbefund dieser Studie wurde die Zulassung für Canakinumab in der kardiovaskulären Therapie nicht weiter verfolgt.11
Parallel wurden mehrere Therapiestudien mit Colchicin durchgeführt, das neben einer Hemmung von Mikrotubuli auch etwas breiter antiinflammatorisch wirkt und insbesondere eine Hemmung des NLRP3-Inflammasoms und seiner Aktivierungsprodukte (IL-1β, IL-6) bewirkt. In LoDoCo2 wurden 5500 Patient:innen mit chronischem Koronarsyndrom entweder mit Low-Dose-Colchicin (0,5mg täglich) oder Placebo behandelt. In einem mittleren Follow-up von 29 Monaten war der kombinierte Endpunkt aus Myokardinfarkt, zerebralem Insult, koronarer Revaskularisierung und kardiovaskulärem Tod um 31% gesenkt, wobei keine erhöhte Rate an Infektionen in der Colchicin-Gruppe festgestellt wurde.12 In COLCOT wurden 4700 Patient:innen mit Myokardinfarkt innerhalb von 30 Tagen und unabhängig von ihrem CRP-Wert eingeschlossen und mit Low-Dose-Colchicin oder Placebo behandelt. Nach einem mittleren Follow-up von 23 Monaten wurde auch hier der kardiovaskuläre Endpunkt um 22% gesenkt.12
Diese positiven Effekte auf kardiovaskuläre Ereignisse konnten jedoch nicht mit allen antiinflammatorisch wirksamen Substanzen nachgewiesen werden. Beispielsweise konnte mit Methotrexat keine Endpunktwirkung erreicht werden. Allerdings wurde auch keine Wirkung auf IL-1β, IL-6 oder CRP nachgewiesen.13 Es ist somit davon auszugehen, dass insbesondere die Inflammasomwirkung von entscheidender Bedeutung für den Therapieerfolg ist. Laufende klinische Studien mit Hemmung von IL-6 werden hier neue mechanistische Einblicke liefern.14
Leitlinienempfehlung für Colchicin
Insbesondere basierend auf LoDoCo2 und COLCOT sollte seitens der aktuellen ESC-Leitlinien von 2024 eine antiinflammatorische Therapie mit Colchicin 0,5mg p.o. einmal täglich bei Patient:innen mit chronischem Koronarsyndrom zur Reduzierung kardiovaskulärer Ereignisse erwogen werden (Klasse-IIa-Empfehlung).15 Diese Empfehlung ist nun unseres Erachtens ein klares und leichter umsetzbares Upgrade im Vergleich zur Empfehlung der ACS-Leitlinien von 2023, wo eine „Add-on“-Therapie mit Colchicin nur bei unzureichend eingestellten Risikofaktoren oder rekurrierenden Ereignissen trotz optimaler medikamentöser Therapie erwogen werden konnte (Klasse-IIb-Empfehlung).16
Während ein residuelles inflammatorisches Risiko am ehesten ab einem hsCRP von >2mg/l angenommen werden kann, kann die Therapie aber unabhängig von einer hsCRP-Messung erfolgen, da die Wirksamkeit in den Studien ebenfalls unabhängig vom hsCRP vorhanden war. Colchicin mit einer geringen Tagesdosis von 0,5mg täglich wird bei guter Nieren- und Leberfunktion als sicher gesehen. Eine Verwendung bei einer schweren Nieren- oder Leberschädigung, Störungen des blutbildenden Systems ist ebenso wie eine Kombination mit CYP3A4-Hemmern oder P-Glykoproteinen zu vermeiden.17
Während derzeit noch keine Zulassung in dieser Indikation durch die europäische Arzneimittelagentur (EMA) erfolgt ist, ist eine Zulassung durch die amerikanische Food and Drug Administration (FDA) bereits im Juni 2023 erfolgt.18 Es bleibt zu erwähnen, dass im November 2024 und somit nach Veröffentlichung der ESC-Leitlinien von 2024 die ersten Daten der CLEAR-SYNERGY(Oasis 9)-Studie publiziert wurden. Hier konnte bei mehr als 7000 randomisierten Patient:innen nach Myokardinfarkt und erfolgter Koronarintervention durch Low-Dose-Colchicin-Therapie nach 5 Jahren keine signifikante Reduktion schwerer kardiovaskulärer Ereignisse festgestellt werden.19 Aufgrund möglicher Einflüsse durch die Covid-19-Pandemie sowie fraglich ausreichender Senkung des hsCRPs in dieser Studie ist ohne weitere Analysen eine Einordnung dieser Studiendaten aktuell schwierig.20
Ausblick in die Zukunft
Praxistipp
Eine Colchicin-Gabe von 0,5 mg pro Tag p. o. sollte nach ESC zur Senkung der kardiovaskulären Ereignisrate bei Patient:innen mit chronischem Koronarsyndrom als antiinflam-matorische Therapie erwogen werden, sofern keine Kontraindikation wie schwere Nieren-/Leberfunktionsstörung, Störungen des blutbildenden Systems bzw. keine kombinierte Einnahme mit CYP3A4-Hemmern oder P-Glykoproteinen vorliegt.Daten aus der Grundlagenforschung sowie erste Ergebnisse klinischer Studien deuten darauf hin, dass eine Hemmung des IL-6-Signalwegs sowie die direkte Hemmung des NLRP3-Inflammasoms Erfolg versprechende neue Therapiekonzepte darstellen könnten.21,22 Ein weiteres attraktives Konzept wäre eine Impfung gegen Atherosklerose. Bei der Entstehung der Atherosklerose kommt es zur Bildung von Autoantikörpern gegen z.B. LDL, oxidiertes LDL und ApoB sowie zur Vermehrung von T-Zellen, die ApoB-100 in oxidierten LDL-Partikeln erkennen. Eines der möglichen Konzepte bei der Entwicklung einer Impfung ist beispielsweise eine Immunisierung mit ApoB-Peptiden, die dann zur Ausbildung einer protektiven Immunität gegenüber ApoB führt.23,24
Die Forschungs- und Studienaktivität im Bereich der kardiovaskulären Inflammation und Immunologie lässt erwarten, dass weitere antiinflammatorische Therapien in der Zukunft verfügbar sein werden, um die kardiovaskulären Ereignisraten von Patient:innen mit koronarer Herzerkrankung weiter senken zu können.
Literatur:
1 Wolf D, Ley K: Immunity and inflammation in atherosclerosis. Circ Res 2019; 124(2): 315-27 2 Horstmann H et al.: Cross-species single-cell RNA sequencing reveals divergent phenotypes and activation states of adaptive immunity in human carotid and experimental murine atherosclerosis. Cardiovasc Res 2024; 120(14): 1713-26 3 Hansson GK et al.: Inflammation and plaque vulnerability. J Intern Med 2015; 278(5): 483-93 4 Fahed AC, Jang IK: Plaque erosion and acute coronary syndromes: phenotype, molecular characteristics and future directions. Nat Rev Cardiol 2021; 18(10): 724-34 5 Hedar AM et al.: Autoimmune rheumatic diseases and vascular function: the concept of autoimmune atherosclerosis. J Clin Med 2021; 10(19): 4427 6 Peikert A et al.: Residual inflammatory risk in coronary heart disease: incidence of elevated high-sensitive CRP in a real-world cohort. Clin Res Cardiol 2020; 109(3): 315-23 7 Bohula EA et al.: Inflammatory and cholesterol risk in the FOURIER trial. Circulation 2018; 138(2): 131-40 8 Ridker PM et al.: Reduction in C-reactive protein and LDL cholesterol and cardiovascular event rates after initiation of Rosuvastatin: a prospective study of the JUPITER trial. Lancet 2009; 373(9670): 1175-82 9 Ridker PM et al.: Antiinflammatory therapy with Canakinumab for atherosclerotic disease. N Engl J Med 2017; 377(12): 1119-31 10 Ridker PM et al.: Relationship of C-reactive protein reduction to cardiovascular event reduction following treatment with Canakinumab: a secondary analysis from the CANTOS randomised controlled trial. Lancet 2018; 391(10118): 319-28 11 https://ec.europa.eu/health/documents/community-register/html/h564.htm 12 Nidorf SM et al.: Colchicine in patients with chronic coronary disease. N Engl J Med 2020; 383(19): 1838-47 13 Ridker PM et al.: Low-dose methotrexate for the prevention of atherosclerotic events. N Engl J Med 2019; 380(8): 752-62 14 ClinicalTrials.gov. https://clinicaltrials.gov/study/NCT05021835 15 Vrints C et al.: 2024 ESC Guidelines for the management of chronic coronary syndromes. Eur Heart J 2024; 45(36): 3415-537 16 Byrne RA et al.: 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J 2023; 44(38): 3720-826 17 Nidorf SM et al.: Low-dose colchicine for atherosclerosis: long-term safety. Eur Heart J 2024; 45(18): 1596-1601 18 O’Neill L (für AGEPHA Pharma): U.S. FDA approves first anti-inflammatory drug for cardiovascular disease. https://us.agephapharma.com/blog/2023/06/20/us-fda-approves-first-anti-inflammatory-drug-for-cardiovascular-disease ; zuletzt aufgerufen am 5.2.2025 19 Jolly SS et al.: Colchicine in acute myocardial infarction. N Engl J Med 2024; doi:10.1056/NEJMOA2405922 20 Tardof JC et al.: Efficacy and safety of colchicine and spironolactone after myocardial infarction: the CLEAR-SYNERGY trial in perspective. Eur Heart J Acute Cardiovasc Care 2024; 13(12): 843-4 21 Ridke PM et al.: IL-6 inhibition with ziltivekimab in patients at high atherosclerotic risk (RESCUE): a double-blind, randomised, placebo-controlled, phase 2 trial. Lancet 2021; 397(10289): 2060-9 22 Zahid A et al.: Pharmacological inhibitors of the NLRP3 inflammasome. Front Immunol 2019; 10: 487654 23 Wolf D et al.: Pathogenic autoimmunity in atherosclerosis evolves from initially protective apolipoprotein B100-reactive CD4+T-regulatory cells. Circulation 2020; 142(13): 1279-93 24 Kobiyama K et al.: Vaccination against atherosclerosis. Curr Opin Immunol 2019; 59: 15-24
Das könnte Sie auch interessieren:
Neue Daten aus dem VERTIS-Studienprogramm
Die kardiovaskuläre Sicherheitsstudie VERTIS CV mit dem SGLT2-Inhibitor Ertugliflozin verlief weniger günstig als andere Endpunktstudien zu dieser Substanzgruppe. Die Hintergründe dafür ...
Liraglutid - Hoffnung auf Betazellprotektion
Mit der Kombination eines Immunmodulators mit dem GLP-1-Analogon Liraglutid konnte in einer Population von Patienten mit neu diagnostiziertem Typ-1-Diabetes der Verlust an Betazellen ...
DAPA-CKD: Dapagliflozin schützt die Nieren und reduziert die Mortalität
Im Rahmen des EASD-Kongresses wurden erfreuliche Daten zur Nephroprotektion des SGLT2-Inhibitors Dapagliflozin präsentiert. Dieser reduzierte in der Studie DAPA-CKD in einer Population ...