Neues aus der Alzheimer’s Disease Drug Development Pipeline
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der Amyloidpathologie an, die einen von mehreren bekannten pathogenetischen Mechanismen darstellt. Der Artikel fasst die aktuelle, sehr dynamische Landschaft der in Entwicklung befindlichen Pharmaka in dieser hochprioritären Indikation zusammen.
Die Entwicklung innovativer Pharmakotherapie der Alzheimerkrankheit hat in den letzten Jahren einen bemerkenswerten Aufschwung erfahren. Mit der Zulassung der Amyloidantikörper Lecanemab (Leqembi®) und Donanemab (Kisunla®) ist die Erkrankung erstmals ursächlich behandelbar geworden. Wenngleich eine Heilung auch mit diesen Medikamenten nicht erfolgt, bedeutet doch die Verlangsamung des Verlaufs um ca. 30% über 18 Monate einen klinisch relevanten Effekt, der wahrscheinlich mit einer längeren Behandlungsdauer zunimmt. Die besten Ergebnisse lassen sich bei einem frühen und sehr frühen Therapiebeginn erzielen, idealerweise noch im Stadium der milden kognitiven Störung. Die Verfügbarkeit dieser Substanzen in der Klinik stellt zweifellos einen Paradigmenwechsel in der Behandlung der Alzheimerkrankheit dar.
Verfügbare Amyloidantikörper
Beide Substanzen setzen an dem als zentral in der Pathogenese der Erkrankung angesehenen Protein Aß42 an, das sich als Amyloid in der Hirnrinde in den senilen Plaques ablagert. Die sog. Amyloid-Kaskaden-Hypothese besagt, dass dieser Vorgang der initiale Zündmechanismus der Neurodegeneration ist, der dem Eintreten anderer Pathomechanismen und erster klinischer Symptome um ca. 2 Dekaden vorausgeht. Die Amyloid-Kaskaden-Hypothese gilt heute als weitgehend bestätigt. Während Donanemab an den Plaques selbst ansetzt, richtet sich Lecanemab hauptsächlich gegen sog. Protofibrillen, die als eine Vorstufe der Amyloidablagerungen angesehen werden.
Sowohl Lequembi® als auch Kisunla® werden als i.v. Infusion alle 2 Wochen bzw. alle 4 Wochen über 1,5 Jahre bzw. bis zur Erreichung von Amyloidnegativität in der Positronen-Emissions-Tomografie (PET) verabreicht. Eine strenge Patientenselektion, aufwendige bildgebende und molekulare Diagnostik, mehrere MRT-Kontrollen zum Ausschluss von „amyloid-related imaging abnormalities“ (ARIAs) während der Therapie und hohe Kosten machen die Behandlung nur einer eingeschränkten Patientengruppe zugänglich. Sie kann derzeit in Österreich ausschließlich im intramuralen Bereich verabreicht werden.
Durchbruch erfolgt, Ziel teilweise erreicht
Die folgenden Ziele sind aktueller Gegenstand intensiver Forschung im universitären und industriellen Bereich:
1. Optimierung der schon verfügbaren Antiamyloidtherapien durch Erweiterung auf noch frühere Erkrankungsstadien (präklinisch), Senkung des Therapieaufwands, Steigerung der Wirkung und Vermeidung der limitierenden Nebenwirkungen, im Besonderen der ARIA
2. Entwicklung neuer therapeutischer Strategien durch Beeinflussung anderer in der Pathogenese der Alzheimerkrankheit beteiligter Prozesse, (z.B. Tau-Pathologie, Entzündung etc.)
3. Entwicklung von Kombinationstherapien, die dem multifaktoriellen Entstehungsmechanismus Rechnung tragen
4. Steigerung der Gehirngesundheit und Resilienz, Prävention
Pipeline
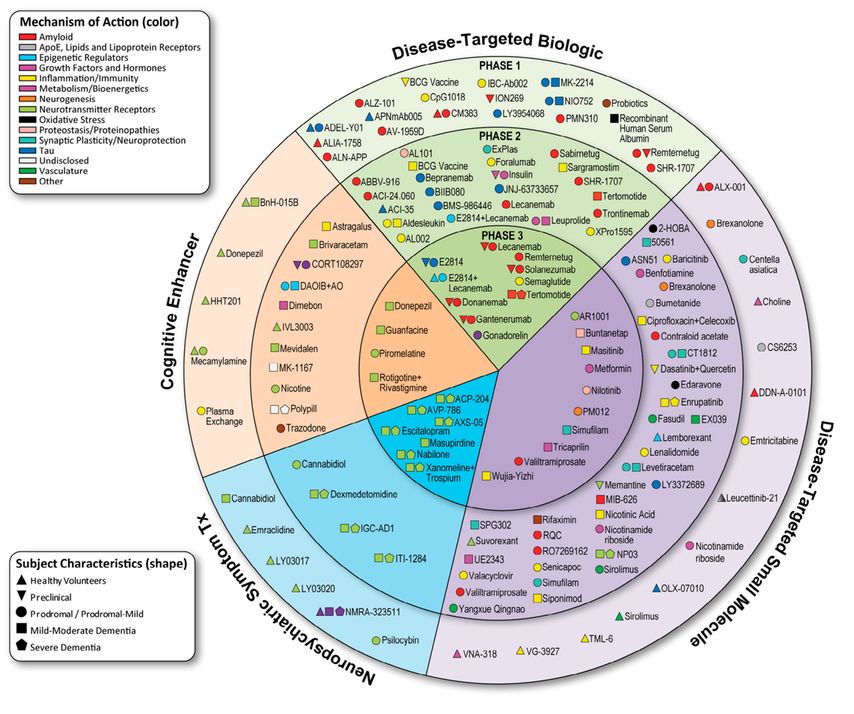
Die aktuelle Pipeline (Stand 1/2025) umfasst 138 Substanzen, die in 182 klinischen Studien am Menschen untersucht werden und an 15 verschiedenen biologischen Mechanismen angreifen. Etwa ein Drittel dieser Medikamente ist in anderen Indikationen bereits zugelassen (sog. „drug repurposing“). 31 Substanzen befinden sich in Phase III der Entwicklung (Abb.1). Weltweit sind mehr als 50000 Patienten in diesen Studien eingeschlossen.
Abb. 1: Pipeline 2025 für die Entwicklung von Alzheimermedikamenten (aus Cummings JL et al.: Alzheimer’s disease drug development pipeline: 2025. Alzheimers Dement (N Y) 2025; 11(2): e70098. doi: 10.1002/trc2.70098)
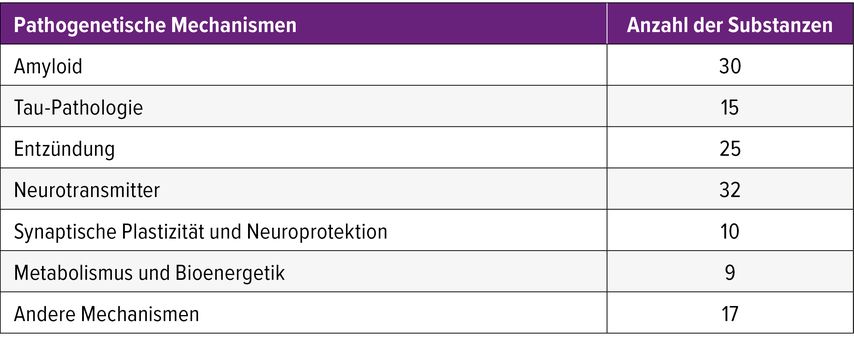
Die meisten untersuchten Substanzen adressieren die in Tabelle 1 angegebenen pathogenetischen Mechanismen.
Die Vielfalt der Angriffspunkte unterstreicht die Komplexität der Pathogenese der Alzheimerkrankheit, die sich nicht auf einen einzelnen Mechanismus beschränkt.
Was ist in der mittelfristigen Zukunft zu erwarten?
1. Amyloidantikörper der zweiten Generation
-
Die s.c. Formulierung von Lecanemab als Erhaltungstherapie mit Verabreichung alle 4 Wochen nach den ersten 1,5 Behandlungsjahren ist von der FDA bereits zugelassen (Leqembi Iqlik®, Fa. Eisai) und bei der EMA eingereicht.
-
Eine s.c. Formulierung einer Weiterentwicklung von Donanemab (Remtermetug, Fa. Eli Lilly) mit noch höherer Plaque-reduzierender Potenz befindet sich in Phase III der klinischen Entwicklung.
-
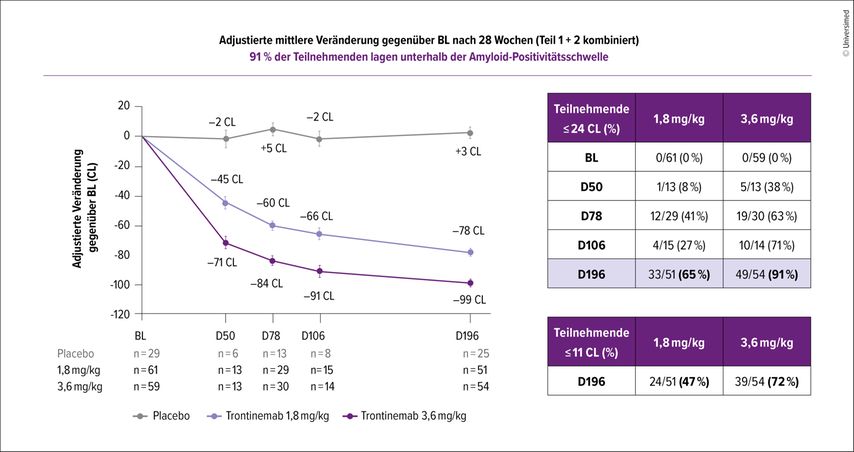
Der monoklonale Antikörper Trontinemab (Fa. Roche) ist an ein sog. „brain shuttle“ gekoppelt, mithilfe dessen die Substanz die Blut-Hirn-Schranke durchdringt. Damit können bis zu 18-fach höhere Konzentrationen im Hirngewebe erzielt werden. Damit steigt der Amyloid-reduzierende Effekt und es sind niedrigere systemische Dosen erforderlich, was zu einer sehr deutlichen Reduktion der oft limitierenden ARIAs führt (Abb. 2). Trontinemab befindet sich in Phase III und eine Zulassung 2028/2029 scheint realistisch.
Abb. 2: Dosisabhängige biologische Wirkung des Amyloidantikörpers Trontinemab (dzt. Entwicklungsphase III) auf die Amyloidpathologie gemessen mit der Positronen-Emissions-Tomografie. Das rasche und effiziente Clearing der Amyloidablagerungen ist Voraussetzung für die klinische Wirkung (modifiziert nach Kulic L. et al.: Oral Presentation at AAIC, Toronto, July 2025)
2. Tau-Therapeutika
Die Ablagerungen und transsynaptische Ausbreitung von pathologisch phosphoryliertem Tau in den Neuronen werden als ein wesentlicher Mechanismus des Neuronentods angesehen und korrelieren gut mit dem Ausprägungsgrad der klinischen Symptome. Während die meisten Studien mit Antikörpern gegen Tau (z.B. Semorinemab, Gosuranemab) als Monotherapie bislang keine konsistenten klinischen Effekte zeigen konnten, haben kürzlich die folgenden neuen Antikörper, die gegen die Mikrotubulus-bindende Region von Tau gerichtet sind, von der FDA eine „fast track designation“ zur weiteren Entwicklung erhalten.
-
Etalanetug (Fa. Eisai), untersucht in Kombination mit Lecanemab, zeigt Wirkung auf den Blutbiomarker MTBR-tau243.
-
BMS-986446 (Fa. Bristol Myers Squibb) wurde gleichfalls gegen dieses Epitop entwickelt.
-
Posdinemab (Fa. Johnson & Johnson) ist gegen p-tau 217 gerichtet.
-
Alle Substanzen zeigen deutliche Wirkung auf die Blutbiomarker Aβ42, p-tau 181 und p-tau 217.
Zulassungsstudien sind in Planung.
Auch aktive Immunisierungen werden untersucht, waren aber bislang ohne klinische Wirkung und verbleiben in frühen Entwicklungsstadien. Der Tau-Aggregationshemmer HMTM (ein Abkömmling des Farbstoffes Methylenblau) hat kürzlich eine positive Phase-III-Studie publiziert und die Daten zur Zulassung in Großbritannien eingereicht.
Eine absehbare Zulassung von Tau-basierten Therapien in der EU ist derzeit nicht am Horizont.
3. Kombinationstherapien
Die Kombination von Medikamenten, die Amyloid-beta reduzieren, mit solchen, die die transsynaptische Ausbreitung von abnorm phosphoryliertem Tau verhindern, gilt als die vielversprechendste Zukunftsstrategie. Erste Studienergebnisse zu kombinierten Immuntherapien gegen Amyloid und Tau werden um 2028 erwartet. Auch die Kombination von Amyloid- und/oder Tau-Antikörpern mit Entzündungsmodulatoren oder Stoffwechselregulatoren wird angedacht. Die wissenschaftliche Community ist sich einig, dass die Alzheimerkrankheit ähnlich wie Krebs oder HIV künftig mit einer Polytherapie behandelt werden muss.
Biomarker-basierte Präzisionstherapie
Die zunehmende Verfügbarkeit von Biomarkern aus dem Blut (z.B. p-tau 181, p-tau 217, MTBR-tau, …) setzt sich zum Ziel, ein molekulares Profil des individuellen Patienten zu erstellen. Diese Marker haben bereits in den Zulassungsstudien Anwendung gefunden und sind die Basis informativer Subgruppenanalysen. Ziel in der Zukunft ist eine personalisierte Präzisionstherapie, die individuell auf das Biomarkerprofil des individuellen Patienten abgestimmt ist.
Cave!
Festzuhalten ist, dass es seit vielen Jahren immer wieder positive oder ermutigende Daten aus Studien der Phase II gibt, die sich aber letztlich in den angeschlossenen großen Zulassungsstudien nicht bestätigen ließen. Auch immer wieder kommunizierte eindrückliche Ergebnisse in Beobachtungsstudien lassen nicht den Rückschluss auf eine therapeutische Wirkung zu. Vor Kurzem zeigte der GLP-1-Rezeptor-Agonist Semaglutid, der in einer Kohortenstudie in den USA an über 1 Million Patienten mit Diabetes Typ 2 im Vergleich mit anderen Antidiabetika mit einer um 40–70% reduzierten Inzidenz von Demenz einherging, in zwei Phase-III-Studien keine Wirkung auf klinischen Verlauf und Biomarker bei Patienten mit MCI oder milder Alzheimerdemenz.
Fazit
-
Mit den seit Kurzem zugelassenen Amyloidantikörpern Lecanemab und Donanemab steht Patienten mit früher Alzheimerkrankheit erstmals eine krankheitsmodifizierende Therapie zur Verfügung. Wenngleich nur einer eingeschränkten Patientengruppe zugänglich und mit großem diagnostischem, organisatorischem und finanziellem Aufwand verbunden, so handelt es sich doch um einen Paradigmenwechsel in der Behandlung der Alzheimerkrankheit.
-
Positive Studiendaten haben in den letzten Jahren zu einer deutlichen Zunahme des wissenschaftlichen Interesses und zu vermehrten Investitionen pharmazeutischer Unternehmen geführt. 138 Substanzen befinden sich in unterschiedlichen Phasen klinischer Entwicklung.
-
In den nächsten wenigen Jahren ist damit zu rechnen, dass die Weiterentwicklung der Amyloid-basierten Therapien zu weniger aufwendigen Therapieschemata (im Besonderen subkutane Verabreichung und längere Dosierungsintervalle) und besserer Verträglichkeit (z.B. Trontinemab) führen wird.
-
In Hinblick auf Entwicklungen jenseits dieses Mainstreams laufen zahlreiche, zum Teil vielversprechende klinische Studien, die vordergründig die Tau-Pathologie, aber auch andere pathogenetische Mechanismen adressieren. In der Klinik erwarten wir allerdings aus dieser Forschungsrichtung keine neuen Zulassungen in absehbarer Zeit.
-
Nach dem ersten Erfolg der Amyloid-basierten Therapien erfährt die Alzheimerpipeline derzeit einen deutlichen Aufschwung und Wendepunkt mit der Entwicklung zahlreicher neuer Substanzen. Ziel ist eine an den individuellen Patienten und sein Biomarkerprofil angepasste personalisierte Therapie im frühesten Stadium.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Whatʼs new in glioma: from molecular insights to clinical innovations
The landscape of glioma research has evolved over the past decade, bridging fundamental neurobiology with clinical applications. From spatial tumor architecture to AI-powered diagnostics ...
Parkinsonprävention durch Lebensstilmodifikation
Noch bevor die ersten motorischen Symptome der Parkinsonkrankheit auftreten, beginnt die Erkrankung auf biologischer Ebene. Auch wenn bislang keine pharmakologische Neuroprotektion oder ...
Ist die ketogene Diät eine Präzisionsmedizin?
Die ketogenen Ernährungstherapien sind etablierte Behandlungsformen bei Epilepsie. Während sie primär bei therapierefraktären pädiatrischen Epilepsien eingesetzt werden, finden sie ...