Ist die ketogene Diät eine Präzisionsmedizin?
Autorinnen:
Dr. med. Andrea Rüegger
Prof. Dr. med. Georgia Ramantani, PhD
Abteilung Neuropädiatrie
Universitäts-Kinderspital Zürich
Medizinische Fakultät
Universität Zürich
E-Mail: andrea.rueegger@kispi.uzh.ch
Die ketogenen Ernährungstherapien sind etablierte Behandlungsformen bei Epilepsie. Während sie primär bei therapierefraktären pädiatrischen Epilepsien eingesetzt werden, finden sie zunehmend auch Anwendung bei einem breiteren Spektrum pädiatrischer und adulter Epilepsien sowie weiteren neurologischen Krankheitsbildern. Angesichts dieser Indikationserweiterung stellt sich die grundlegende Frage nach dem therapeutischen Ansatz: Handelt es sich um eine individualisierte Therapie oder ein standardisiertes Konzept?1
Präzisionsmedizin
Präzisionsmedizin ist aktuell ein zentrales Thema und hat in den letzten Jahren insbesondere bei der Behandlung von Epilepsien grosse Aufmerksamkeit erfahren. Präzisionstherapien werden synonym auch als personalisierte oder individualisierte Therapien bezeichnet. Neben dem individuellen Genom sollten dabei auch Umweltfaktoren sowie sozioökonomische, psychologische und biologische Daten in die Therapieentscheidung einbezogen werden.2 Hierfür bedarf es valider Biomarker, um jene Patienten zu identifizieren, die optimal auf eine ketogene Ernährungstherapie ansprechen.
Metabolische Grundlagen
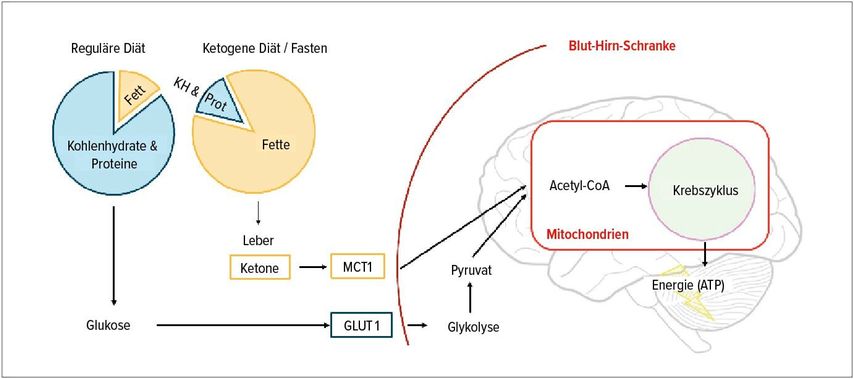
Das Prinzip ketogener Diäten besteht darin, dem Gehirn Fett in Form von Ketonkörpern anstelle von Glukose als primären Energieträger bereitzustellen. Während eine herkömmliche Ernährung auf Kohlenhydraten und der daraus gewonnenen Glukose basiert, führt die ketogene Diät (ähnlich wie das Fasten) zur hepatischen Produktion von Ketonkörpern (β-Hydroxybutyrat, Acetoacetat, Aceton). Entsprechend zeichnen sich ketogene Diätformen durch einen hohen Fett- und einen geringen Kohlenhydratanteil aus (Abb. 1).3
Abb. 1: Fett als alternative Energiequelle für das Gehirn. Aus Fett werden in der Leber Ketonkörper gebildet, die über den MCT1-Transporter die Blut-Hirn-Schranke passieren und in den Mitochondrien der Nervenzellen zu Energie umgewandelt werden
Potenzielle Wirkmechanismen der ketogenen Ernährungstherapien
Um anfallsunterdrückend zu wirken, muss die ketogene Diät die neuronale Hyperexzitabilität und Hypersynchronität reduzieren. Der Diät werden verschiedene Wirkmechanismen zugeschrieben, die bisher jedoch weitestgehend hypothetisch bleiben. Dabei spielt insbesondere das β-Hydroxybutyrat als Signalmolekül eine entscheidende Rolle (Abb. 2).4
Epigenetische Regulation
β-Hydroxybutyrat ist an der Modifikation von Histonproteinen beteiligt, was wiederum den Schutz vor oxidativem Stress verbessert.5
Darmmikrobiom
Das Darmmikrobiom spielt bei einer Vielzahl von Erkrankungen eine entscheidende Rolle. Studien konnten belegen, dass die ketogene Diät die Diversität der Darmflora moduliert und diese Veränderung zum anfallsunterdrückenden Effekt der Diät beiträgt.6 Zudem deutet Evidenz auf eine spezifische Korrelation zwischen der Mikrobiom-Zusammensetzung und der Epileptogenese hin. So weisen insbesondere Säuglinge mit therapierefraktärer Epilepsie ein charakteristisches Mikrobiom-Profil auf, das sich deutlich von gesunden Kontrollgruppen abhebt.7 Die Analyse des Darmmikrobioms hat somit ein vielversprechendes Potenzial für die Etablierung künftiger Biomarker.
Oxidativer Stress und Neuroinflammation
Neuroinflammatorische Prozesse, die insbesondere die Aktivierung von Mikroglia- und Astroglia-Zellen beinhalten, sind entscheidende Faktoren bei der Entstehung und Progression von Epilepsien. Die ketogene Diät wirkt über verschiedene Mechanismen antiinflammatorisch und neuroprotektiv.8
Ketonkörper
Trotz umfangreicher Datenlage bleibt bisher ungeklärt, ob die Ketonkörper selbst einen direkten anfallsunterdrückenden Effekt ausüben.9 Es gibt jedoch Evidenz für ihre neuroprotektive Wirkung.10
Ansprechen auf die ketogenen Ernährungstherapien
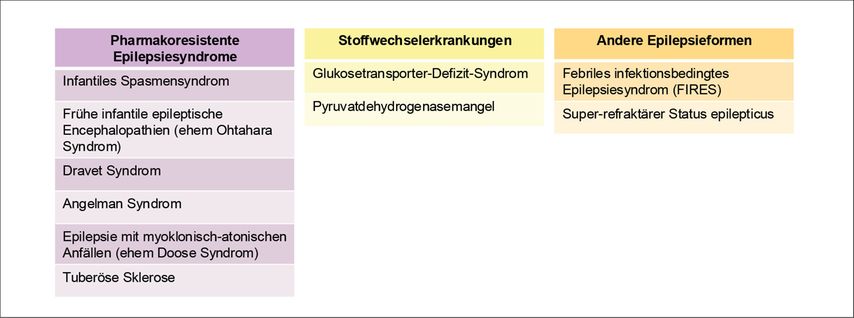
Diverse Studien belegen die Wirksamkeit ketogener Diäten bei verschiedenen Epilepsiesyndromen und epileptischen Erkrankungen (Abb. 3).3 Dabei zeigte sich bei der Mehrheit der Patienten eine Anfallsreduktion. Dieser Effekt tritt jedoch nicht bei allen Patienten gleichermassen ein und ist selbst bei Patienten mit der identischen Grunderkrankung nicht immer konstant.11,12
Abb.3: Ketogene Ernährungstherapien werden bei verschiedenen Epilepsien und genetischen Syndromen als effektiv beschrieben. Diese lassen sich in 3 Gruppen aufteilen: pharmakoresistente Epilepsiesyndrome, Stoffwechselerkrankungen und andere Epilepsieformen (adaptiert nach Kossoff EH et al., Epilepsia Open 2018)3
Ein besonderer Stellenwert kommt dem Glukosetransporter-Defizit-Syndrom (GLUT1-DS) zu. Dies ist eine metabolische Erkrankung, bei der eine lebenslange ketogene Diät erforderlich ist. Aufgrund des defekten Glukosetransportproteins im Gehirn ist das Organ auf Ketonkörper als alternative Energiequelle angewiesen. GLUT1-DS ist mit verschiedenen Epilepsiephänotypen, Bewegungsstörungen sowie kognitiven Einschränkungen assoziiert. Ein frühzeitiger Beginn der ketogenen Diät führt hier zu einer signifikanten Verbesserung der Symptomatik und in den meisten Fällen zu einer vollständigen Anfallskontrolle.13,14 In diesem Kontext stellt die ketogene Diät eine gezielte, individualisierte Therapie dar. Dennoch bleibt die Kernfrage der klinischen Praxis bestehen: Wie lässt sich prädiktiv bestimmen, welche Patienten optimal auf diese alternative Therapieform ansprechen?
Personalisierung durch Biomarker und «Omics»-Technologien
Um die Patientengruppe, die optimal auf eine ketogene Diät anspricht (die sogenannte ketogene-Diät-sensitive Population), präzise zu identifizieren, ist die Identifizierung valider Biomarker unerlässlich. Aktuell sind diese Marker noch nicht hinreichend bekannt, doch die Forschungsaussichten sind vielversprechend. Innovative Ansätze untersuchen derzeit die Auswirkungen der ketogenen Ernährungstherapie auf die Genexpression über verschiedene «Omics»-Ebenen – dazu zählen unter anderem Genomik, Metabolomik und Proteomik.15 Diese Daten könnten künftig dabei helfen, den Therapieerfolg individuell vorherzusagen.
Schlussfolgerung
Zusammenfassend lässt sich festhalten, dass ketogene Ernährungstherapien eine wirksame alternative Behandlungsform für verschiedene Epilepsiesyndrome darstellen und zunehmend erfolgreich bei weiteren neurologischen Erkrankungen eingesetzt werden. Die grösste klinische Herausforderung bleibt jedoch die präzise Identifizierung jener Patienten, die am stärksten von dieser Therapie profitieren. Es bleibt zu hoffen, dass durch die Fortschritte in der Biomarker-Forschung und der Systembiologie in naher Zukunft verlässliche Parameter zur Verfügung stehen, um die ketogene Diät als festen Bestandteil einer personalisierten Präzisionsmedizin zu etablieren.
Literatur:
1 Falsaperla R et al.: Is ketogenic diet a ‘precision medicine’? Recent developments and future challenges. Eur J Paediatr Neurol 2024; 48: 13-6 2 Delpierre C, Lefèvre T: Precision and personalized medicine: What their current definition says and silences about the model of health they promote. Implication for the development of personalized health. Front Sociol 2023; 8: 1112159 3 Kossoff EH et al.: Optimal clinical management of children receiving dietary therapies for epilepsy: updated recommendations of the International Ketogenic Diet Study Group. Epilepsia Open 2018; 3(2): 175-92 4 Zhu H et al.: Ketogenic diet for human diseases: the underlying mechanisms and potential for clinical implementations. Signal Transduct Target Ther 2022; 7(1): 11 5 Shimazu T et al.: Suppression of oxidative stress by β-hydroxybutyrate, an endogenous histone deacetylase inhibitor. Science 2013; 339(6116): 211-4 6 Olson CA et al.: The gut microbiota mediates the anti-seizure effects of the ketogenic diet. Cell 2018; 173(7): 1728-41.e13 7 Fang S et al.: The comparison of gut microbiota between different types of epilepsy in children. Microb Cell Fact 2025; 24(1): 64 8 Dupuis N et al.: Ketogenic diet exhibits anti-inflammatory properties. Epilepsia 2015; 56(7): e95-e8 9 Masino SA, Rho JM: Mechanisms of ketogenic diet action. Jasper’s Basic Mechanisms of the Epilepsies [Internet]. 4th ed. 2012 10 Ma W et al.: Ketogenic diet metabolites reduce firing in central neurons by opening KATP channels. J Neurosci 2007; 27(14): 3618-25 11 Falsaperla R et al.: Toward a working definition of ketogenic diet resistance in GLUT1 deficiency syndrome. Epileptic Disord 2025; 27(6): 1247-54 12 Falsaperla R et al.: Exploring ketogenic diet resistance in glucose transporter type 1 deficiency syndrome: a comprehensive review and critical appraisal. Epilepsia Open 2025; 10(1): 31-9 13 Kass HR et al.: Use of dietary therapies amongst patients with GLUT1 deficiency syndrome. Seizure 2016; 35: 83-7 14 Auvin S: Targeted therapies in epilepsies. Rev Neurol 2025; 181(5): 450-5 15 Liu Y et al.: Ketogenic therapy towards precision medicine for brain diseases. Front Nutr 2024; 11: 1266690
Das könnte Sie auch interessieren:
Parkinsonprävention durch Lebensstilmodifikation
Noch bevor die ersten motorischen Symptome der Parkinsonkrankheit auftreten, beginnt die Erkrankung auf biologischer Ebene. Auch wenn bislang keine pharmakologische Neuroprotektion oder ...
Pharmakologische und neuromodulatorische Behandlungen des Clusterkopfschmerzes
Die Behandlung des chronischen Clusterkopfschmerzes steht noch heute vor großen Herausforderungen. Am 19. European Headache Congress (EHC) 2025 präsentierte Dr. Anja Petersen, ...
Neues aus der Alzheimer’s Disease Drug Development Pipeline
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der ...