DGN-2025-Wrap-up: Biomarkerdiagnostik und Behandlungder Alzheimerkrankheit in der klinischen Praxis
Bericht:
Felix Schmidtner, MSc
Auch beim diesjährigen Kongress der Deutschen Gesellschaft für Neurologie (DGN) waren die Fortschritte in der Behandlung der Alzheimerdemenz ein gefragtes Thema. Zur Biomarkerdiagnostik referierte Prof. Dr. Thomas Duning, Chefarzt der Klinik für Neurologie Bremen, während Dr. Monika Köchling vom Medizinischen Versorgungszentrum Neuro-Centrum Grevenbroich über die Behandlung in der Praxis sprach und darüber, wie Neurolog:innen vor Ort gezielt Strukturen für die Behandlung mit den neuen krankheitsmodifizierenden Präparaten schaffen können.
Alzheimer und andere Demenzformen sind Volkskrankheiten, die mit großem Leid für die Betroffenen und ihre Angehörigen einhergehen. Auch wenn die Effektstärken der ersten zugelassenen krankheitsmodifizierenden Medikamente gegen die Alzheimerdemenz kleiner sein mögen, als manche Ärzte und Ärztinnen erhofft haben, so stellen sie dennoch einen Paradigmenwechsel dar.
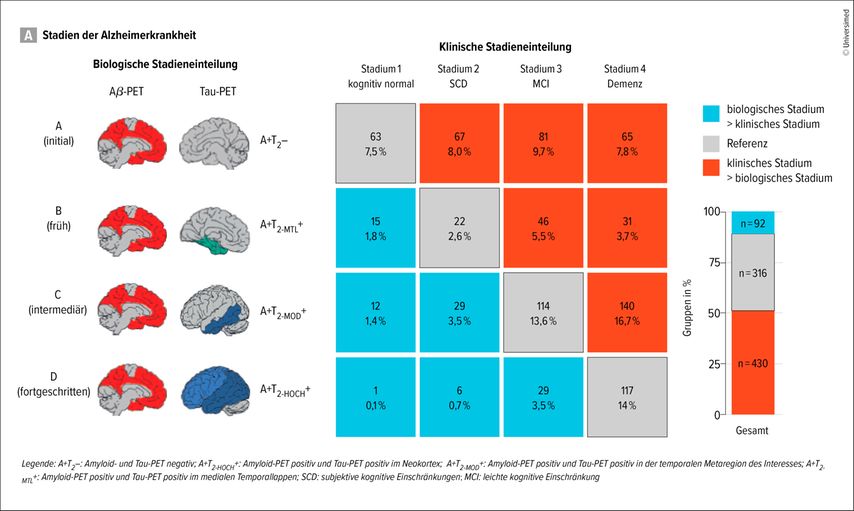
Prof. Dr. Duning ist seit 2021 Chefarzt an der Klinik Bremen-Ost und leitete bereits Phase-II- und Phase-III-Studien zur Behandlung der Alzheimerdemenz in Münster. Beim DGN-Kongress 2025 gab er einen praxisnahen Überblick über den Status quo und die Aussichten der Biomarkerdiagnostik. „Für die neuen Therapieoptionen ist es wichtig, dass wir die Diagnose früh stellen, da die neuen Medikamente bereits im frühen Stadium ansetzen sollen. Dafür müssen wir die Biomarker bestimmen“, so Duning. Während die Alzheimerkrankheit noch langsam voranschreitet, können andere Bereiche des Gehirns die ersten Defizite kompensieren. Daher ist es bereits zu spät, wenn die volle klinische Symptomatik der Alzheimerkrankheit sichtbar ist. Duning sieht selbst im Stadium der leichten kognitiven Störung (MCI) ein klinisches Spätstadium (Abb.1)1.
Abb. 1: Biologische und klinische Stadien im Vergleich anhand der schwedischen Studienkohorte BioFINDER-2 (modifiziert nach Binette AP et al.)1
Geschichte der Biomarker
Was die Geschichte der Biomarker betrifft, blickt Duning zurück auf die erste Bestimmung der Alzheimerkrankheit. Als Alois Alzheimer, damals „Irrenarzt“ in München, toxische Veränderungen im Gehirn seiner kürzlich verstorbenen Patientin Auguste Deter aufzeichnete, beschrieb er mit den Amyloid-Plaques mit der Aminosäurenlänge 42 praktisch den ersten Biomarker.2 Heute kennen wir neben Amyloid-β-42 die Ratiomarker sowie die Tau-Marker Gesamt-Tau und Phospho-Tau-Protein. „Die Ratios sind sensitiver als Amyloid-β-42 alleine, generell sind die zur Verfügung stehenden Biomarker aber exzellent“, so Duning. Zur Veranschaulichung verweist er auf die Washington Health Study.3 Im Rahmen der Studie von Long et al. wurden Personen in einem Alter von Anfang 50 liquorpunktiert und über 25 Jahre nachverfolgt. Mit einer Spezifizität von 94,1% und einer Sensitivität von 87,0% konnte vorausgesagt werden, ob eine Person eine Alzheimerdemenz entwickeln würde oder nicht. Daher können und sollen bereits die leicht betroffenen Patient:innen auf Biomarker getestet werden und nicht erst die mittelgradig oder schwer betroffenen. Dies hat auch in die aktuelle S3-Leitlinie zur Diagnostik der Alzheimerdemenz Eingang gefunden, wofür Duning Lob von amerikanischen Kolleg:innen bekommt.4 Die Verlässlichkeit der Biomarker haben Dr. Ayda Rostamzadeh und Prof. Dr. Frank Jessen vom Deutschen Zentrum für neurodegenerative Erkrankungen bereits 2020 untersucht: Wenn ein Patient heute einen positiven Liquornachweis für pathologische Amyloid- und Tau-Werte hat, liegt die Wahrscheinlichkeit, dass der Patient in fünf Jahren eine Alzheimerdemenz entwickelt, bei 90%.5
Alternativen zur Liquorpunktion
Der Amyloid-PET liefert ebenfalls sehr gute Ergebnisse (Spezifizität 0,81%, Sensitivität 0,91%),6 aufgrund der hohen Kosten sieht Duning für die flächendeckende Anwendung jedoch wenig Potenzial. Zum Einsatz von blutbasierten Biomarkern gab es 2024 eine spannende Studie aus Schweden. Dabei wurden blutbasierte Biomarker in einem Hausarztsetting bei zwei Kohorten mit rund 200 bzw. 400 Patient:innen erhoben. Sie zeigten eine Genauigkeit von einem „Area under the curve“-Wert von 96% bzw. 97%.7 Von der amerikanischen Food and Drug Administration wurde 2025 bereits der erste blutbasierte Biomarker zugelassen.8 Duning ist sich sicher, dass eine Zulassung in Europa folgen wird – jedoch müssen noch etwaige Bedenken ausgeräumt werden, bevor sich die Europäische Arzneimittelbehörde (EMA) entscheiden wird. Für das höchstsensitive Tau-PET sieht Duning dahingegen wenig Potenzial: Dieses ist noch teurer als das Amyloid-PET und die Anwendung ist aufwendig, die Tracer zerfallen in kürzester Zeit, so Duning. Zumal Tau-PET-Diagnostik aktuell in Deutschland nur von vier Zentren regelmäßig zur Alzheimerdiagnostik angeboten werde. Zukunft sieht er dafür im Einsatz von Digitalen Gesundheitsanwendungen (DiGAs). In einer breiten US-amerikanischen Studie der Firmen Apple und Biogen, die 2024 im Journal Nature Medicine erschienen ist, konnte bei über 20000 Patient:innen anhand der Daten von Smartwatches bestimmt werden, ob eine Person an MCI erkrankt ist oder nicht.9 Dabei wurden passive Daten wie die Handynutzung (Tipp- und Telefonverhalten), und Gesundheitsparameter (Puls- und Schlafdaten) kombiniert mit Daten aus kognitiven Tests, die ebenso am Handy durchgeführt wurden. Aus europäischer Perspektive mit Auge auf den Datenschutz wirken solche Studien delikat, aber sie veranschaulichen gut, welches Potenzial DiGAs für eine Vorfilterung haben.
Für die Zukunft hofft Duning, dass mithilfe von Biomarkerdiagnostik gepaart mit nichtmedikamentösen Präventivstrategien und den neuen krankheitsmodifizierenden Therapien das Auftreten alltagsrelevanter Defizite, bei denen Betroffene Pflege rund um die Uhr benötigen, erheblich reduziert werden kann.
Vernetzung als Schlüssel für neue Alzheimertherapien in der Praxis
Dr. Monika Köchling aus Grevenbroich fährt fort mit einem praxisnahen Einblick, wie man die Behandlung vor Ort mit den neuen kausalen Therapien gestalten kann. Am Neuro-Centrum Grevenbroich hatte man bereits Erfahrungen mit Infusionen für die Multiple-Sklerose-Therapie, was für die neuen Antikörpertherapien gegen Alzheimer half. Ein Schlüssel ist für Köchling das Stichwort Vernetzung. Am Ende des Tages ist weniger der Platz, sondern das Personal bei großem Andrang der limitierende Faktor.
In Grevenbroich wurde daher ein Netzwerk mit den Hausärzt:innen in der Umgebung, kooperierenden Ärzten, Spitälern in der Nähe und der Radiologie geschaffen. Eine medizinische Fachangestellte (MFA) hat ein eigenes Ansprechtelefon für Kolleg:innen und Patient:innen. Mit der benachbarten Radiologiepraxis konnte vereinbart werden, dass direkt Slots für die MRT-Untersuchung eingebucht werden können. Lokal wurde bereits ein Demenzboard etabliert, in dem auch knifflige Fälle besprochen werden können – wenn beispielsweise keine klare Alzheimerdemenz vorliegt, sondern eine isolierte Tau-Pathologie.
Für die Praxis – insbesondere mit der gestiegenen öffentlichen Präsenz der Krankheit Demenz – ist eine sinnvolle Vorauswahl essenziell. Schließlich würde es zu viele Ressourcen binden, wenn jede Person mit subjektiven kognitiven Einschränkungen liquorpunktiert würde. Eine ausgiebige neuropsychologische Diagnostik wie bspw. mit der CERAD-Testbatterie kann bereits im Vorfeld Hinweise auf Alzheimer- oder eine andere Demenzform geben.10,11Um dem erhöhten Bedarf an neuropsychologischen Testungen gerecht zu werden, investierte das Neuro-Centrumin die Fort- und Weiterbildung der Mitarbeiter:innen.
Ein weiterer Punkt in der Praxis, der nicht unterschätzt werden sollte, ist das Infusionsmanagement. Die Patient:innen müssen schließlich in der Regel lange nachbeobachtet werden, was wiederum Ressourcen bindet. Je nach Therapie gibt es unterschiedliche Intervalle: Lecanemab-Infusionen erfolgen alle zwei Wochen, Donanemab-Infusionen alle vier Wochen. Die Österreichische Alzheimer Gesellschaft empfiehlt bei den ersten zwei Infusionen von Lecanemab eine Nachbeobachtungszeit von fünf Stunden, bei Donanemab eine Nachbeobachtungszeit von zwei Stunden.12,13
„Darüber hinaus ist wichtig, Bescheid darüber zu wissen, was die Symptome von allergischen und infusionsbedingten Reaktionen sind“, erklärt Köchling. Hinweise könnten Rötung um die Einstichstelle, Kopfschmerzen, Fieber, Schüttelfrost, Übelkeit und Erbrechen, Blutdruckveränderungen, Schwitzen, Engegefühl im Brustkorb und Atemnot sein.14,15 Ärzt:innen sollten mit Rückfragen zu möglichen Nebenwirkungen wie den bekannten Bildanomalien („amyloid-related imaging abnormalities“, ARIA) seitens der Patient:innen rechnen und wissen, wann diese Grund zur Sorge sind. ARIA sind zwar in den meisten Fällen (74–97%) asymptomatisch und sind auch in den Kontrollgruppen aufgetreten,16 jedoch erfordern sie eine sorgfältige Beobachtung und Kontrolle. Mögliche klinische Symptome einer ARIA können Kopfschmerzen, Verwirrtheit, Übelkeit/Erbrechen, Seh- und Sprechstörungen, Schwindel, Krampfanfälle, Zittern und Bewusstseinsänderungen sein.14–16 Bei leichten, asymptomatischen ARIA kann unter Abwägung die Behandlung fortgesetzt werden, bei moderaten ARIA muss unter derzeitigem Kenntnisstand die Therapie unterbrochen werden. Wenn sich 2–4 Monate später die ARIA mit Ödembildung (ARIA-E) rückbildet bzw. sich die ARIA mit Hämosiderinablagerung (ARIA-H) stabilisiert, kann eine Fortsetzung der Therapie erwogen werden.15 Solche Entscheidungen können in einem lokalen Demenzboard besprochen werden.
Für Lecanemab ist vor Therapiebeginn, vor der dritten, fünften, siebten und 14. Infusion ein Kontroll-MRT vorgesehen, für Donanemab muss neben dem zerebralen MRT vor Beginn der Behandlung eine Kontrolluntersuchung vor der zweiten, dritten, vierten und siebten Infusion eingeplant werden. Als Nachschlagewerk empfehlen Köchling und Duning das Alzheimer Qualitätshandbuch der deutschen Berufsverbände für Neurologie, Psychiatrie und Nervenheilkunde (BDN/BVDP/BVDN), in dem die Inhalte der S3-Leitlinie zur Behandlung von Demenzen praxisnah zusammengefasst sind.17 Außerdem führt das Neuro-Centrum Grevenbroich laufend Schulungen für MFAs durch, an denen Interessierte teilnehmen können.
Quelle:
Kongress der Deutschen Gesellschaft für Neurologe (DGN) 2025 vom 12.–15.11.2025 in Berlin; Vorträge von Thomas Duning und Monika Köchling am 12.11.2025
Literatur:
1 Binette AP et al.: Evaluation of the revised criteria for biological and clinical staging of Alzheimer disease. JAMA Neurol 2025; 82(7): 666-75 2 Alzheimer A: Über eine eigenartige Erkrankung der Hirnrinde. Allgemeine Zeitschrift für Psychiatrie und psychisch-gerichtliche Medizin 1907; 64: 146-7 3 Long JM et al.: Preclinical Alzheimer’s disease biomarkers accurately predict cognitive and neuropathological outcomes. Brain 2022; 145(12): 4506-18 4 DGN e.V. & DGPPN e.V: (Hrsg.): S3-Leitlinie Demenzen, Version 5.2, 17.07.2025, verfügbar unter https://register.awmf.org/de/leitlinien/detail/038-013 , zuletzt aufgerufen am 8.01.26 5 Rostamzadeh A, Jessen F: Früherkennung der Alzheimer-Krankheit und Demenzprädikation bei Patienten mit leichter kognitiver Störung. Zusammenfassung aktueller Empfehlungen. Nervenarzt 2020; 91: 832-42 6 Ruan D, Sun L: Amyloid-β PET in Alzheimer’s disease: a systematic review and Bayesian meta-analysis. Brain Behav 2023; 13(1): e2850 7 Palmqvist S et al.: Blood biomarkers to detect Alzheimer disease in primary care and secondary care. JAMA 2024; 332(15): 1245-57 8 U.S. Food and Drug Administration: Pressemitteilung vom 16. Mai 2025, abrufbar unter: https://www.fda.gov/news-events/press-announcements/fda-clears-first-blood-test-used-diagnosing-alzheimers-disease , zuletzt aufgerufen am 8.01.2026 0 9 Butler PM et al.: Smartwatch- and smartphone-based remote assessment of brain health and detection of mild cognitive impairment. Nat Med 2025; 31(3): 829-39 10 Künig G et al.: The impact of the CERAD-NP on diagnosis of cognitive deficiencies in late onset depression and Alzheimer’s disease. Int J Geriatr Psychiatry 2006; 21(10): 911-6 11 Diehl J et al.: Frontotemporal dementia, semantic dementia, and Alzheimer‘s disease: the contribution of standard neuropsychological tests to differential diagnosis. J Geriatr Psychiatry Neurol 2005; 18(1): 39-44 12 Österreichische Alzheimer Gesellschaft: Donanemab SOP/ÖAG Version 1, 11/2025, abrufbar unter: https://alzheimer-gesellschaft.at/donanemab-sop-oeag/ , zuletzt aufgerufen am 9.1.2026 13 Österreichische Alzheimer Gesellschaft: Lecanemab SOP/ÖAG Version 1, 11/2025, abrufbar unter: https://alzheimer-gesellschaft.at/donanemab-sop-oeag/ , zuletzt aufgerufen am 9.1.2026 14 Eli Lily: Fachinformation Kisunla 350 mg, Stand September 2025 15 Eisai: Fachinformation Leqembi 100 mg/ml Konzentrat zur Herstellung ener Infusionslösung. Stand: September 2025 16 Cogswell PM et al.: Alzheimer disease anti-amyloid immunotherapies: imaging recommendations and practice considerations for monitoring of amyloid-related imaging abnormalities. AJNR Am J Neuroradiol 2025; 46(1): 24-32 17 Projekt-Arbeitsgruppe Alzheimer Qualitätshandbuch der drei Berufsverbände der Fächer Neurologie, Psychiatrie und Nervenheilkunde (BDN/BVDP/BVDN): Alzheimer Qualitätshandbuch. Abrufbar unter: https://alzheimer-qualitaetshandbuch.de
Das könnte Sie auch interessieren:
APOE und Anti-Amyloid-Therapien: Genetik im klinischen Alltag
Mit der Zulassung der ersten krankheitsmodifizierenden Therapien hat ein Paradigmenwechsel in der Behandlung der Alzheimerkrankheit begonnen. Anti-Amyloid-Antikörper können den ...
Alternative und sequenzielle Migräneprophylaxen im Fokus
Für Migränepatient:innen, die nicht auf gegen das „calcitonin gene-related peptide“ gerichtete monoklonale Antikörper (Anti-CGRP-mAbs) ansprechen, sind alternative Behandlungen und ...
Visualizing focal chronic inflammation in multiple sclerosis: paramagnetic rim lesions and slowly expanding lesions
With increasing awareness of the progression independent of clinical relapses, imaging plays an increasingly important role in the monitoring of people with multiple sclerosis. This ...