Phänotypisierung vor der Asthmatherapie?
Bericht:
Mag. Andrea Fallent
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Auch wenn der Trend bei Asthma eindeutig in Richtung individualisierter Therapie mit Phänotypisierung geht, sind nicht alle Experten davon überzeugt, dass eine routinemäßige Messung verschiedener Biomarker für die Therapieentscheidung essenziell ist. Anlässlich des ERS in Barcelona wurde in der Online-Session„T2 high and T2 low asthma: should we care, or should we only care about asthma?“ zum Thema „Phänotypisierung vor der Asthmatherapie: pro und contra“ debattiert.
Viele Patienten mit schwerem Asthma qualifizieren sich für mehr als ein Biologikum. Bisher gibt es allerdings keine direkten Vergleichsstudien, um die Auswahl zu erleichtern. Post-hoc-Analysen haben jedoch bestimmte klinische Merkmale identifiziert, die mit einem überlegenen Ansprechen auf einige Therapien verbunden sind. Das Vorhandensein von allergischen und/oder eosinophilen Komorbiditäten wie atopischer Dermatitis oder nasaler Polyposis, die zusätzlich von der Wahl des Biologikums profitieren können, sollte ebenso berücksichtigt werden wie Patientenpräferenzen.
Ob die Bestimmung spezifischer Biomarker bei der Diagnosestellung bzw. vor der initialen und/oder Biologika-Therapie für die Praxis wirklich hilfreich ist, wird unterschiedlich bewertet. Ein Befürworter ist ERS-Referent Prof. Dr. Guy Brusselle, Gent. Er integriert in seiner aktuellen Publikation „Biologic Therapies for Severe Asthma“ u.a. Biomarker in den Therapie-Algorithmus von unkontrolliertem schwerem Asthma und präsentierte diese Vorgangsweise auch in seinem Vortrag.1
Pro-Contra-Diskussionsrunde
Vor und nach einer Pro-Contra-Diskussionsrunde beim ERS-Kongress 2022 zur Frage „Should we phenotype bevor treating asthma?“ mit Prof. Dr. Celeste Michala Porsbjerg (pro), Kopenhagen, und Univ.-Prof. Dr. Marco Idzko (contra), Wien, wurde im Auditorium online abgestimmt. 86% stimmten anfangs pro Phänotypisierung, nur 14% dagegen.
Pro Phänotypisierung
Die Argumente für eine Phänotypisierung liegen laut Porsbjerg auf der Hand: „Asthma ist sehr heterogen, alle Patienten gleich zu behandeln, wäre nicht effektiv. Eine Phänotypisierung vor Therapiebeginn erleichtert das effiziente Management.“ Da eine Behandlung mit inhalativen (ICS) oder oralen Kortikosteroiden (OCS) die Biomarker FeNo und Eosinophile verändert, komme die Bestimmung der inflammatorischen Biomarker nur vor dem Einsatz infrage. Das ist laut Porsbjerg dennoch ein obligatorischer Parameter der Diagnostik, insbesondere in Bezug auf allergische Faktoren wie der allergischenRhinitis und hinsichtlich des Type-2(T2)-Asthmas. Porsbjerg: „Die Therapie der allergischen Rhinitis verbessert die Asthmakontrolle, die allergenspezifische Immuntherapie reduziert das Risiko für eine Verschlechterung des Asthmas auch noch neun Jahre danach.“
Als wesentliche Biomarker für die klinische Praxis nannte Porsbjerg Eosinophile und FeNO, um den inflammatorischen Phänotyp zu bestimmen, aber auch um in der Folge das Risiko für Exazerbationen, das Ansprechen auf die Therapie und die Adhärenz des Patienten einzuschätzen: „Mit FeNO-Monitoring können Exazerbationen signifikant reduziert werden.“2 Und spätestens bei der Therapie von schwerem Asthma würden die Patienten von der vorangegangenen Phänotypisierung profitieren.
Contra Phänotypisierung
„95% der Patienten haben kein schweres Asthma, hier können wir die Therapie auch ohne Phänotypisierung beginnen“, entgegnete Idzko. Neutrophiles Asthma (Type-2-low-Asthma) sei ein Mythos, er zitierte dazu die Publikation von Nair P et al. 20213: „Das Vorkommen von Neutrophilen in den Atemwegen reflektiert vermutlich die Dosis der Kortikosteroide oder des Rauchens oder eine Infektion.“ Abgesehen davon werden laut Idzko rund 10% der Asthmapatienten mit OCS und rund 75% mit ICS behandelt: „Wie will man da die Zahl der Eosinophilen bestimmen?“
Die Verlässlichkeit der T2-Asthma-Biomarker sei fraglich: Die Eosinophilenzahl ist abhängig von OCS/ICS-Anwendung bzw. der Zeit der Allergenexposition bei allergischem Asthma, eine mögliche Folge von Begleiterkrankungen wie Infektionen, anderer atopischer Erkrankungen, Neoplasien etc. Ähnliches gelte für den FeNO-Wert. Idzko: „Diese Biomarker funktionieren im Real-Life-Setting nicht. Wir sollten uns um die korrekte Asthmadiagnose kümmern – ist das Asthma schwer bzw. schwierig zu behandeln? – und auf Begleiterkrankungen achten.“ Für die Therapieentscheidung bei schwerem Asthma mit Antikörpern reichen eine entsprechende Anamnese und die Differenzierung von allergischem, nichtallergischem eosinophilem Asthma, der Allergenexposition und der Begleitsymptomatik wie Polyposis nasi und Urtikaria.
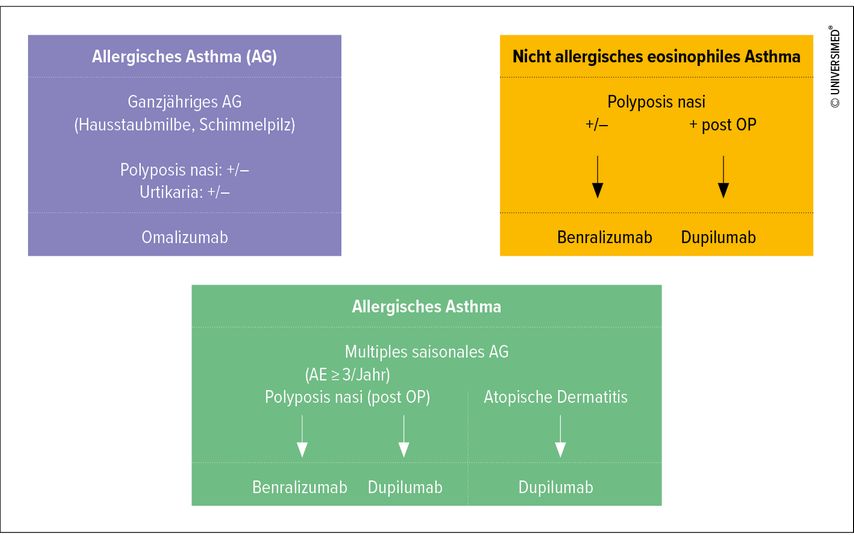
Idzkos Resümee: Phänotypisierung ist wunderbar für wissenschaftliche Studien, für die tägliche Praxis eignet es sich nicht, weil die Biomarker dafür von vielen Faktoren beeinflusst werden und daher wiederholte Messungen notwendig wären. Für die Behandlung von schwerem Type-2-Asthma ist die Komorbiditäten berücksichtigende klinische Therapie indiziert (Abb. 1).
Abb. 1: Schweres (T2-)Asthma: Therapie unter Berücksichtigung klinischer Komorbiditäten (modifiziert nach Idzko M, ERS 2022)
Abschließend stimmten übrigens 64% des Auditoriums pro Phänotypisierung vor der Therapie, und 36% dagegen.
Quellen:
“T2 high and T2 low asthma: should we care, or should we only care about asthma?”, Pro-Con-Debatte von Prof. Dr. Celeste M. Porsbjerg, Kopenhagen, und Univ.-Prof. Dr. Marco Idzko, Wien, beim ERS am 4. September 2022 in Barcelona
Literatur:
1 Brussele G, Koppelman G: Biologic therapies for severe asthma. N Engl J Med 2022; 386: 157-71 2 Petsky H et al.: Tailoring asthma treatment on eosinophilic markers (exhaled nitric oxide or sputum eosinophils): a systematic review and meta-analysis. Thorax 2018; 73(12): 1110-9 3 Nair P et al.: Neutrophilic asthma: misconception or misnomer? Lancet Respir Med 2021; 9(5): 441-3
Das könnte Sie auch interessieren:
Asthma bronchiale: Herausforderungen bei Kindern und Jugendlichen
Asthma bronchiale ist eine chronische Krankheit, die im Kindesalter andere Herausforderungen mit sich bringt als bei Erwachsenen. Die physikalische Untersuchung sowie die Therapie sind ...