Revolutionieren Stammzellen die ästhetische Medizin?
Autorin:
Univ.-Prof. Dr. Hildegard T. Greinix
Klinische Abteilung für Hämatologie
Medizinische Universität Graz
E-Mail: hildegard.greinix@medunigraz.at
Regenerative Stammzelltherapie hat es sich zum Ziel gesetzt, Entzündungen natürlich zu unterbinden und geschädigtes Gewebe von innen heraus abheilen zu lassen. Wie der menschliche Körper selbst, verwendet die regenerative Medizin Stammzellen, um die Erholung von beschädigten Zellen und Geweben zu stimulieren. Die Stammzelltherapie geht dabei über herkömmliche Methoden zur Reparatur und Regeneration alters- bzw. krankheitsbedingter Schäden hinaus, indem die Stammzellen u.a. potenziell Gewebe und Organe in einen gesünderen Zustand zurückversetzen sollen.
Stammzellen (SZ) zeichnen sich durch unbegrenzte Selbsterneuerung sowie die Möglichkeit der Differenzierung in reifere Gewebe und Zellen aus, wobei sie sich je nach Entwicklungspotenzial nur in Zellen der Gewebe entwickeln können, in denen sie sich befinden, oder sich auch in andere Gewebe transdifferenzieren können. Während sich pluripotente Stammzellen zu unterschiedlichen Organen entwickeln können, sind adulte Stammzellen multipotent und bereits auf ein Organ festgelegt. Adulte Stammzellen regenerieren stark beanspruchte Körpergewebe wie Haare, Haut, Muskel, Knochen, Knorpel und Schleimhäute lebenslang.
Ein wissenschaftlich nachgewiesener Benefit ist bisher nur für die klinische Anwendung hämatopoetischer Stammzellen im Rahmen der Blutstammzelltransplantation (HSZT) als kurative Therapie für Patienten mit akuten Leukämien, Lymphomen und Myelomen sowie die Gabe von SZ zur Regeneration der Haut nach schweren Verbrennungen und Regeneration der Cornea durch die Verabreichung entsprechender Stammzellen dokumentiert.
Hautstammzellen und deren klinische Anwendung
Auch in der humanen Haut gibt es wie in anderen Geweben Stammzellen. Haarfollikel-Stammzellen sind in den äußeren Schichten der Haarbälge lokalisiert und können nach Transplantation differenzierte Haarfollikelabkömmlinge etablieren. Epidermale Stammzellen sitzen in der Basalschicht und differenziertere Zellen wandern in höhere Hautschichten. Melanozyten-Stammzellen stammen vom Neuralrohr ab und finden sich zusammen mit Haarfollikel-Stammzellen in den Haarbälgen. Die Stammzellen der Talg- und Schweißdrüsen sind in der myoepithelialen und luminalen Schicht der Schweißdrüsen lokalisiert und proliferieren nur sehr selten.
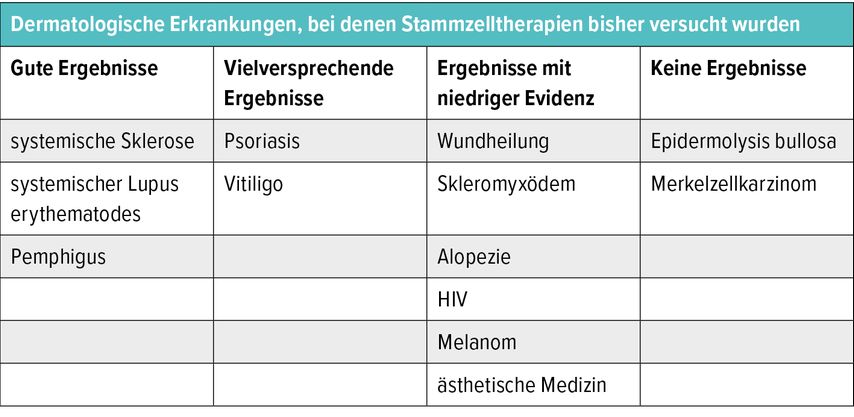
Tabelle 1 zeigt die dermatologischen Erkrankungen, bei denen bishereine Stammzelltherapie versucht wurde. Gute Ergebnisse wurden bei Autoimmunerkrankungen wie der systemischen Sklerose oder dem systemischen Lupus erythematodes nach Hochdosisimmunsuppression und Verabreichung hämatopoetischer Stammzellen erzielt, während bei vielen anderen Erkrankungen sehr fragwürdige Ergebnisse vorliegen.
Tab. 1: Dermatologische Erkrankungen, bei denen Stammzelltherapien bisher versucht wurden (modifiziert nach Kandhpur S et al.)5
Eine rezente Publikation, die 64 randomisierte Studien mit 2888 Patienten analysierte, fand, dass die häufigsten Indikationen die androgene Alopezie (45%), Vitiligo (31%) und die Alopecia areata waren.1 In diesen klinischen Studien wurde eine Vielzahl an Methoden angewandt, wobei am häufigsten thrombozytenreiches Plasma (56%), die Transplantation autologer epidermaler Melanozyten/Keratinozyten (19%), die isolierte Transplantation von Melanozyten (6%) und die Transplantation von Zellen aus dem Haarfollikel (5%) genannt wurden. Daneben wurden mesenchymale Stromazellen (MSZ) (2%), konzentrierte Wachstumsfaktoren, Konditionierungsmedium aus unterschiedlichen Zellkulturen, Extrakte aus Adipozyten-Stammzellen und vieles mehr klinisch angewandt. MSZ haben bestimmte Oberflächenmerkmale, differenzieren in vitro in Osteoblasten, Adipozyten und Chondrozyten und können aus unterschiedlichen Geweben wie Knochenmark, Nabelschnurblut, Skelettmuskel, Plazenta oder Fettgewebe gewonnen werden.
Präklinische Studien zeigten, dass MSZ einen hohen Stellenwert bei der Hautregeneration und Verjüngung haben könnten, da sie antiinflammatorische und immunmodulierende Wirkung haben, Kollagen und Elastin synthetisieren, die Aktivierung von Metalloproteinasen inhibieren und vor UV-Licht-induzierter Seneszenz schützen.2 Die Stammzellen der Adipozyten stellen eine Form der MSZ dar, finden sich in der stromalen vaskulären Fraktion (SVF) des Fettgewebes, bewirken parakrine Effekte und fördern die Angiogenese und Wundheilung.3 Sie werden mittels Aspiration bei der Fettabsaugung gewonnen. Da die Isolation der Adipozyten-SZ aufwendig ist, wird klinisch meist die SVF verwendet, die sich aus Adipozyten-SZ, Präadipozyten, Perizyten, hämatopoetischen Zellen, Fibroblasten, Endothelzellen, glatten Muskelzellen und Immunzellen zusammensetzt.
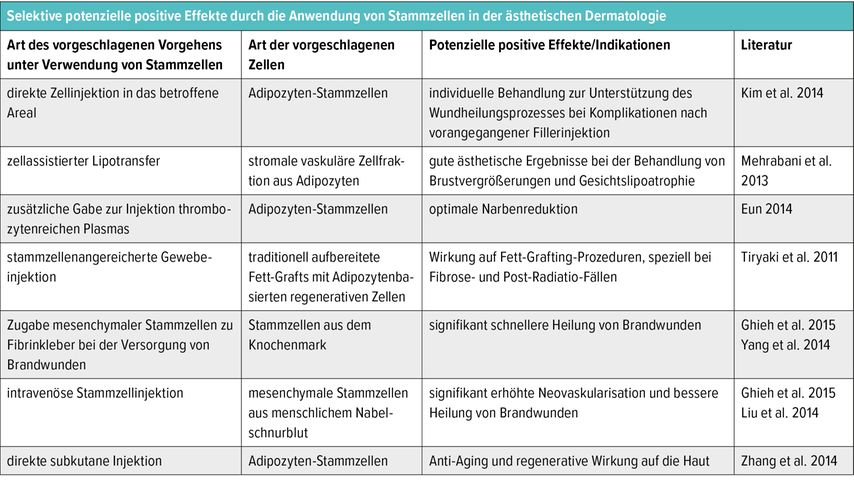
Tabelle 2 zeigt mögliche positive Effekte der Anwendung von SZ in der ästhetischen Dermatologie.
Tab. 2: Selektive potenzielle positive Effekte durch die Anwendung von Stammzellen in der ästhetischen Dermatologie (modifiziert nach Nowacki M et al.)6
Neuerdings werden auch Exosomen, die 40–100nm große extrazelluläre Vesikel darstellen und von allen Geweben sezerniert werden können und auch von MSZ, Adipozyten-SZ und hämatopoetischen SZ stammen können, vermehrt beforscht. Exosomen werden von der endosomalen Membran generiert und enthalten multiple Proteine, Lipide und Nukleinsäuren. Sie regulieren die Proliferation, Differenzierung, Migration, Apoptose und interzelluläre Kommunikation der Zellen und ihre Sezernierung hängt vom Aktivierungszustand der Zellen ab, sodass ein und dieselbe Zelle unterschiedliche Exosomen bilden kann.4 Auch für Hautexosomen ist eine Vielzahl an Funktionen aus präklinischen Studien beschrieben. Deren klinische Anwendung ist derzeit noch mit vielen Herausforderungen assoziiert, wie Verbesserung der Isolation von Exosomen, deren Heterogenität, die die Reproduzierbarkeit therapeutischer Effekte in klinischen Studien erschwert, und den Defizit präklinischer Modelle in Hinblick auf humane dermatologische Erkrankungen.
Herausforderungen der Stammzelltherapie in der ästhetischen Medizin
Tausende Gruppen weltweit versuchen, Produkte aus Stammzellen oder stammzellbasierte Interventionen zu vermarkten, wobei viele fälschlicherweise als stammzellbasiert angepriesen werden, klinisch jedoch noch nicht entsprechend erprobt und geprüft sind und damit neben Kunden-/Patiententäuschung auch Gesundheitsrisiken darstellen könnten. In vielen Ländern und Regionen gibt es auch noch keine gesetzlichen Regulationen, um Kunden zu schützen und eine entsprechende Qualität und Sicherheit der angepriesenen Produkte zu gewährleisten.
Da Stammzellen als „lebende Medikamente“ anzusehen sind, die unterschiedliche Effekte nach In-vivo-Verabreichung bewirken können, sollte unbedingt darauf geachtet werden, dass Labors, die Stammzellen bearbeiten, nach strengen Regeln der Qualitätskontrolle tätig sind, entsprechende Protokolle vorlegen, die eine Reproduzierbarkeit von Ergebnissen ermöglichen, und die Substanzen, die in vivo verabreicht werden, auch möglichst gut definiert sind. Dies betrifft alle Arbeitsschritte wie Zellgewinnung und -isolation, Zellkultivierung, Selektionen und andere Manipulationen, die phänotypischen Charakteristika der Zellen, Zellkonzentrationen im finalen Produkt und die Verabreichungsmodi. Auch sind adäquate klinische Studien für jede Form der stammzellbasierten Therapie unbedingt erforderlich, um deren Sicherheit und Wirksamkeit verglichen mit Placebo oder anderen etablierten Therapien zu bestätigen.
Zusammenfassung
Insgesamt muss sicherlich festgehalten werden, dass stammzellbasierte Produkte schon seit Jahren weltweit vermarktet werden, ohne dass entsprechende Sicherheits- und Wirksamkeitsdaten vorliegen, und dass die Nachfrage nach ihnen weiter zunimmt.
Die Forschung hat auf dem Gebiet der Stammzellbiologie in den vergangenen Jahren beeindruckende Fortschritte erzielt. So stellt die HSZT für ausgewählte Patienten mit benignen und malignen hämatologischen Erkrankungen oft die einzige kurative Therapieoption dar und ist weltweit als klinischer Standard etabliert. Auch die Pathophysiologie dermatologischer Erkrankungen ist zunehmend besser beforscht, sodass neue innovative Therapiestrategien basierend auf diesen Erkenntnissen entwickelt werden können. Die Verwendung von Stammzellen oder stammzellbasierten Produkten in der ästhetischen Medizin sollte nicht als trivial abgetan werden, da Stammzellen komplexe biologische Entitäten, sog. „living drugs“ darstellen und durch den Medienhype große Hoffnungen in deren Wirkung gesetzt werden. Patienten erwarten sich Veränderungen in ihrer Selbstwahrnehmung und ihrem „body image“, die zu einer Verbesserung ihrer Lebensqualität beitragen, und sollten auch aus Sicht des Konsumentenschutzes nur in Produkte investieren, von denen sie berechtigterweise eine Verbesserung ihrer Beschwerden erwarten können. Daher sollte die kosmetische Industrie nicht nur in die Entwicklung neuer Produkte zur unmittelbaren Anwendung investieren, sondern gerade im Bereich der stammzellbasierten Therapien gute wissenschaftliche klinische Daten vorlegen können, um die klinische Anwendung bestimmter Produkte evidenzbasiert zu rechtfertigen und den Erwartungshaltungen der Kunden/Patienten zu entsprechen. Daneben würden diese neuen wissenschaftlichen Ergebnisse zu weiteren bedeutenden Erkenntnissen im Bereich der Stammzellbiologie führen und die gesamte medizinische Community in ihrem Bestreben, die vielfältigen Wirkungen von Stammzellen optimal in der Klinik zum Wohle der Patienten einzusetzen, entscheidend unterstützen.
Literatur:
1 Jafarzadeh A et al.: Regenerative medicine in the treatment of specific dermatologic disorders: a systematic review of randomized controlled clinical trials. Stem Cell Res Ther 2024; 15: 176 2 Jo H et al.: Application of mesenchymal stem cells in skin regeneration and rejuvenation. Int J Mol Sci 2021; 22: 2410 3 Semsarzadeh N, Khetarpal S: Rise of stem cell therapy in aesthetics. Clin Dermatol 2022; 40: 49-56 4 Kose O et al.: Role of exosomes in skin diseases. J Cosmet Dermatol 2022; 21: 3219-25 5 Khandpur S et al.: Stem cell therapy in dermatology. Indian J Dermatol Venereol Leprol 2021; 87: 753-67 6 Nowacki M et al.: The use of stem cells in aesthetic dermatology and plastic surgery procedures. A compact review of experimental and clinical applications. Adv Dermatol Allergol 2017; 34(6): 526-34
Das könnte Sie auch interessieren:
Der freie mikrovaskuläre SCIP zur Radialis-Hebedefektdeckung
Der freie Radialislappen ist insbesondere in der Kopf-Hals-Chirurgie ein bewährter Standard zur Rekonstruktion. Trotz seiner Vorteile bleibt die Versorgung der Lappenentnahmestelle am ...
Lebensqualität durch minimalinvasive funktionelle Gaumenrekonstruktion
Die funktionelle Rekonstruktion im Kopf-Hals-Bereich zählt zu den anspruchsvollsten Aufgaben moderner Chirurgie, da sie zentrale Lebensfunktionen unmittelbar betrifft. Wenn der weiche ...
Einblicke in die Geschichte des Botulinumtoxins
Die Geschichte der Entstehung des Botulinumtoxins ist bemerkenswert: Vom gefürchteten Lebensmittelgift entwickelte es sich zu einem etablierten, weltweit eingesetzten Arzneimittel mit ...