Am Wendepunkt für Alzheimer? Global Launch der Landmarkstudien der Lancet Commission on dementia
Bericht: Felix Schmidtner
Die Hôpitaux Universitaires Genève (HUG) und The Lancet luden nach Genève, um die neuen Landmarkstudien zur Therapie und Diagnose der Alzheimerdemenz vorzustellen. Die Studien sollen die bisherige Wissenslücke schliessen, Standards harmonisieren und Hoffnung für Betroffene bieten. Denn zu oft erhalten Demenzbetroffene keine Behandlung.
Volle Aufmerksamkeit für AlzFheimer! Pünktlich zum kalendarischen Herbstbeginn regnete es kräftig in Genève. Der Saal des grössten Spitals der Schweiz, der HUG, ist dennoch gefüllt. Schliesslich fand man selten eine solch hochkarätige Speakerliste abseits internationaler Konferenzen. Neben Prof. Dr. med. Giovanni Frisoni von den HUG, der die neue Studienserie koordinierte, sprachen Prof. Dr. med. Richard Horton, Editor-in-Chief von The Lancet, Prof. Dr. med. Frank Jessen vom Deutschen Zentrum für Neurodegenerative Erkrankungen (DZNE), Prof. Dr. med. Nick Fox vom University College London sowie Dr. Katrin Seeher von der WHO.
Die Lancet Commission on dementia wurde 2017 gegründet. Die Arbeit der Commission führte bereits zu mehreren Reports, die das Risiko und Präventionspotenzial für Alzheimerdemenz genauer bezifferten. «Ein Kritikpunkt war, dass wir Diagnose und Therapie aussparten», so Richard Horton, «diese Lücke möchten wir mit der neuen Serie schliessen und Hoffnung für die Betroffenen bieten.» Horton, der auch Honorarprofessor an der London School of Hygiene & Tropical Medicine ist, ist der dienstälteste Editor-in-Chief von The Lancet und initiierte zahlreiche Commissions, um das Fachwissen zusammenzufassen und Aufmerksamkeit für wichtige Themen der Medizin über die Fachgrenzen hinaus zu schaffen. Zuletzt machte die Commission on dementia mit dem Ergebnis auf sich aufmerksam, dass mit der Reduktion von 14 Risikofaktoren 45% des Demenzrisikos modifizierbar sind1. Horton sieht Alzheimer als eine «stealth disease» an. Alzheimer entwickle sich schleichend unter dem Radar, bevor die Krankheit ausbreche. Und die aktuellen Zahlen sind alarmierend: «Wir sehen einen deutlichen Anstieg an ‹disability-adjusted life years› sowie einen ausserordentlichen Anstieg der Sterblichkeit und Krankheitslast», so Horton. Bis 2050 wird Alzheimer von Platz 7 der tödlichsten Krankheiten auf Platz 4 wandern, gleichzeitig wird sich die Krankheitslast verdoppeln. Hinzu kommt, dass die Diagnose Alzheimer oft mit schlechten Perspektiven verbunden wird. Anders als etwa bei der Diagnose eines Diabetes mellitus oder einer Herzerkrankung hätten die meisten Menschen das Gefühl, dass man bei Alzheimer nichts machen könne. Für viele Krankheiten sanken zudem die standardisierten Todesraten, für Alzheimer jedoch nicht. Robert Mardini, der Direktor der HUG, bezeichnete Hortons Rede als Weckruf. «Die aktuelle Lancet-Serie zu Demenz lädt uns dazu ein, die Alzheimerdefinition neu zu denken», meinte Mardini, der damit insbesondere auf die neuen Erkenntisse zu Biomarkern anspielt.
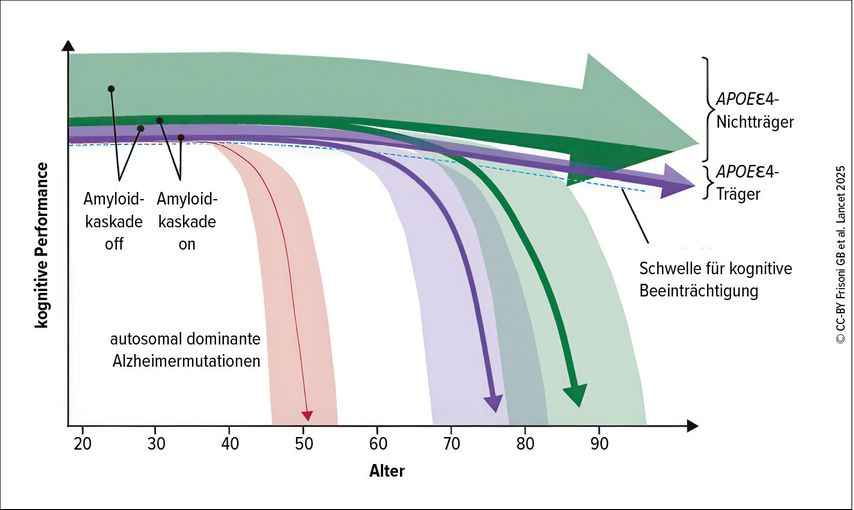
Frank Jessen, Vorsitzender des European Alzheimer’s Disease Consortium (EADC) und Koordinator der deutschen Leitlinie zur Alzheimerkrankheit, stellte die erste der drei neuen Studien der Lancet Commission on dementia vor.2 Jessen arbeitet seit über 30 Jahren an der Krankheit und hat nun erstmals das Gefühl, dass wir uns an einem Wendepunkt der Behandlung und Diagnose der Krankheit befinden. Bis vor einiger Zeit konnten die für die Alzheimerpathologie typischen Veränderungen, die bereits Alois Alzheimer 1906 sah, nur durch Autopsie festgestellt werden. Den Durchbruch brachten die Biomarkerdiagnostik und das PET-Imaging. Zwei Gruppen an Kliniker:innen und Forscher:innen formulierten auf Basis der Biomarkerdiagnostik das Konzept, dass die Alzheimerkrankheit im mittleren Alter startet und die Demenz nur die Endphase der Krankheit bildet.3,4 «Wichtig ist, zu beachten, dass Alzheimer nicht deterministisch ist. Ein grosser Treiber ist zwar die Genetik, Risikogene sind aber sehr rar», erinnerte Jessen. Der APOEε4-Genotyp bestimmt daher viel mehr, in welchem Alter Patient:innen an Alzheimer erkranken, als ob sie überhaupt an Alzheimer erkranken (Abb. 1). Es bleibt daher viel Potenzial, den Ausbruch durch die Modifikation des Lebensstils zu verzögern oder gar zu verhindern.
Abb. 1: Der Ausbruch der Alzheimerkrankheit kann sehr variabel sein. Mit einem patient:innenzentrierten Zugang sind drei verschiedene kognitive Trajektorien ausmachbar: 1 (rot) – Individuen mit autosomal dominanten Alzheimerpathologie-Mutationen, 2 (violett) – Individuen, die homozygote oder heterozygote Träger des APOEε4-Allels sind, 3 (grün) – Nichtträger des APOEε4-Allels, die mit Biomarkern positiv für die Alzheimerpathologie sind (modifiziert nach Frisoni GB et al. 2025)2
Diagnosepfad in drei Wellen
Bisher herrschte ein Disput zwischen den zwei Gruppen, repräsentiert von Clifford Jack et al. und der Alzheimer’s Association Workgroup sowie Bruno Dubois et al. und der International Working Group, inwiefern Biomarker in die Diagnostik integriert werden und gegenüber der klinischen Diagnostik gewertet werden sollen.3,4 Mit der Landmarkstudie der Lancet Commission soll dieser Richtungsstreit nun geklärt werden. Die Autor:innen schlagen eine Diagnostik in drei Wellen vor. In der ersten Welle stehen die Abklärung der Patient:innengeschichte und das erste kognitive Screening im Vordergrund, in der zweiten Welle der Ausschluss anderer Leiden wie eines Deliriums und anderer Krankheitsbilder, denen keine neurodegenerative Veränderung zugrunde liegt. Neben alkoholinduzierten Delirien sind auch Delirien z.B. durch eine Enzephalitis, Herzinsuffizienz oder Infektionen möglich. Ausser erweiterten klinischen Tests und der Blutbildbestimmung können in spezifischen Fällen auch bildgebende Methoden und Biomarker herangezogen werden. Damit soll bereits eine ätiologische Hypothese zur Demenzform (limbisch prädominante altersassoziierte TDP-43-Enzephalopathie [LATE] vs. Alzheimerkrankheit [AD] vs. frontotemporale lobäre Degeneration [FTLD] vs. Lewy-Body-Demenz [LBD] vs. motorische Tauopathie vs. vaskuläre kognitive Einschränkung oder andere neurologische Erkrankungen) formuliert werden. In der dritten Welle sollen dann standardmässig die entsprechenden Biomarker eingesetzt werden, um die ätiologische Hypothese zu bestätigen.
Antikörper sollen Teil eines holistischen Ansatzes werden
Nick Fox vom University College London stellte die zweite Studie der Serie vor, die sich der Behandlung von Alzheimerdemenz widmet.5 «Wir haben gesehen, was Alzheimer mit Familien und Patient:innen anrichtet. Nun können wir endlich in eine neue Ära starten und diese Patient:innen gezielt behandeln», so Fox. Antikörper sind die ersten erfolgreichen krankheitsmodifizierenden Medikamente, die auf eine lange Geschichte gescheiterter Studien folgen. «Die über 18 Monate laufenden Zulassungsstudien zeigten eine dramatische Reduktion der Amyloidakkumulation vor dem Hintergrund, dass sich die Amyloid-β-Pathologie bereits 20 Jahre vorher aufgebaut hat», so Fox. Für Fox ist nun ein holistischer Zugang geboten, indem sowohl nichtpharmakologische Strategien, die symptomatische Therapie mit Cholinesterase-Inhibitoren, und die neuen krankheitsmodifizierenden Medikamente eine Rolle spielen sollten. Gerade die verhaltensbezogenen und psychologischen Symptome werden in der Praxis meist ungenügend beachtet und von Behandler:innen nicht ausreichend adressiert. Dabei könnten die Patient:innen besonders in dieser Hinsicht von nichtpharmakologischen Strategien profitieren. Die möglichen unerwünschten Ereignisse in Verbindung mit Antikörpern möchte Fox dabei nicht kleinreden, mit diversen Vorsichtsmassnahmen wie einer verlangsamten Titration des Antikörpers kann das Risiko für eine «amyloid-related imaging abnormality» (ARIA) jedoch bedeutend reduziert werden.6 Die Effektivität der neuen Medikamente darin, die Progression der Alzheimerkrankheit zu verlangsamen, kann mit den Therapien mithalten, die gegen Krebs, Multiple Sklerose oder rheumatoide Arthritis eingesetzt werden.Fox ist sich sicher: Diese Therapien werden die ersten von vielen neuen krankheitsmodifizierenden Medikamenten gegen Alzheimer sein.
Ein Ende der Kontroverse?
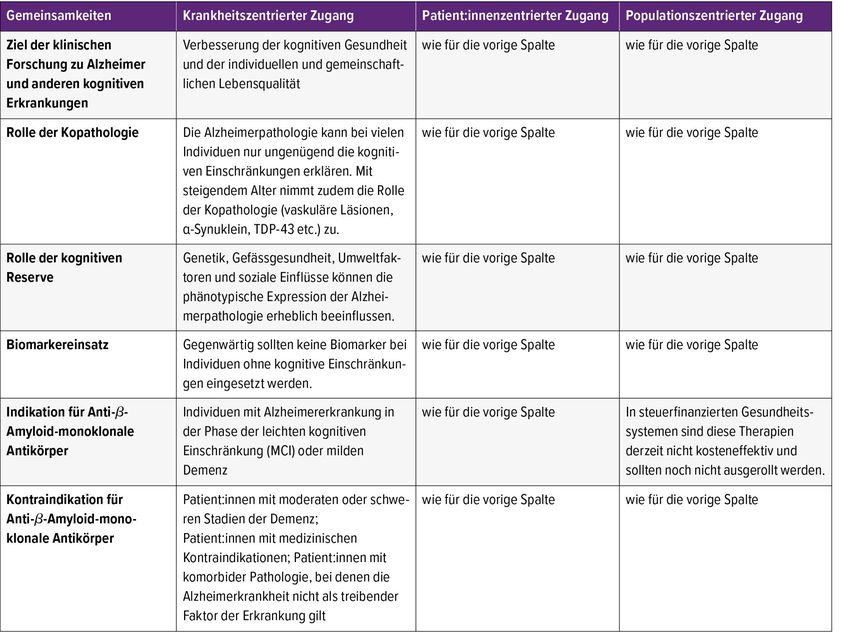
Die dritte Landmarkstudie, die Giovanni Frisoni von den HUG vorstellte, widmet sich der Kontroverse.7 Der Richtungsstreit zwischen biologischer Definition der Alzheimer’s Association und der patient:innenzentrierten Definition der International Working Group wurde bereits von Jessen angesprochen.3,4 Zudem gibt es noch populationszentrierte Ansätze. Für das Paper haben die verschiedenen Expert:innen die Gemeinsamkeiten der verschiedenen Ansätze herausgearbeitet und ausgehend davon Richtungen für die Zukunft formuliert. Dabei ist man sich in den Ansätzen in verschiedenen Gesichtspunkten einig (Tab.1), die Expert:innen sprechen sich unisono gegen den Einsatz von Biomarkern bei Patient:innen ohne kognitive Symptome aus, betonen die Rolle der Kopathologie und der kognitiven Reserve.
Tab. 1: Zentrale Gemeinsamkeiten der verschiedenen Zugänge. Auszug aus Frisoni GB et al. 2025,7 Tabelle 1
Für die Zukunft formulieren die Autor:innen drei Säulen: Risikoassessment, Risikokommunikation und Risikoreduktion. Diese drei Säulen sollen von den Brain Health Services abgedeckt werden und es sollte dabei sowohl die kognitive Reserve, das vaskuläre Risiko als auch das neurodegenerative Risiko adressiert werden.
Zum Schluss sprach Katrin Seeher vom Department für nichtübertragbare Krankheiten der Weltgesundheitsorganisation ein paar Worte. «Diese LandmarkstudienSerie ist eine grosse Chance, den globalen Demenzaktionsplan voranzutreiben», so Seeher. Die Serie biete die Gelegenheit, nun nationale Richtlinien zu standardisieren und zu harmonisieren.
Es stehen also aufregende Zeiten in der Alzheimerbehandlung bevor. Viele Fragen werden die behandelnden Ärzte und Ärztinnen sicher noch länger beschäftigen.
Quelle:
Pressekonferenz von The Lancet und den HUG am 23.9.2025 in Genève
Literatur:
1 Livingston G et al.: Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission. Lancet 2024; 404(10452): 572-628 2 Frisoni GB et al.: New landscape of the diagnosis of Alzheimer’s disease. Lancet 2025; 406: 1389-407 3 Jack CR et al.: Revised criteria for the diagnosis and staging of Alzheimer’s disease. Nat Med 2024; 30(8): 2121-4 4 Dubois B et al.: Alzheimer disease as a clinical-biological construct–an International Working Group recommendation. JAMA Neurol 2024; 81(12): 1304-11 5 Fox NC et al.: Treatment for Alzheimer’s disease. Lancet 2025; 406: 1408-23 6 Wang H et al.: Modified titration of donanemab reduces ARIA risk and maintains amyloid reduction. Alzheimers Dement 2025; 21: e70062 7 Frisoni GB et al.: Alzheimer’s disease outlook: controversies and future directions. Lancet 2025; 406: 1424-42
Das könnte Sie auch interessieren:
Epilepsie: «Wir können heute die Therapie viel mehr individualisieren»
Jahrhundertelang versuchte man, Epilepsiekranken mit Exorzismus ihre angeblichen «Dämonen» auszutreiben. Heute gibt es mehr als 30 wirksame Medikamente, präzisere Diagnostik und neue ...
Migräne: «Wir können alle dazu beitragen, dass die Gesundheitsausgaben nicht ins Unermessliche steigen»
Vor 25 Jahren gab es nur eine Handvoll Medikamente zur Migräneprophylaxe. Heute stehen mit CGRP-basierten Medikamenten in der Schweiz sechs weitere zur Verfügung, sodass mehr Patienten ...
Late-breaking News zur Multiplen Sklerose vom ECTRIMS-Kongress 2025
Der 41. ECTRIMS-Kongress fand dieses Jahr in Barcelona statt. Etwa 9600 Teilnehmer tauschten sich über die neuesten Studiendaten zu Multipler Sklerose und assoziierten Erkrankungen aus. ...