„Left atrial strain“ bei hypertropher Kardiomyopathie
Autoren: Dr. Christopher Mann
Priv.-Doz. DDr. Daniel Dalos, FESC
Klinische Abteilung für Kardiologie
Universitätsklinik für Innere Medizin II
Medizinische Universität Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Vorhofflimmern führt bei Patient:innen mit hypertropher Kardiomyopathie (HCM) häufig zu einem abrupten Einbruch der Belastbarkeit und erfordert nicht selten eine Therapie. Die funktionelle Beurteilung des linken Vorhofs mittels Analyse des „left atrial strain“ erlaubt eine frühere Risikoabschätzung und kann helfen, Patient:innen mit erhöhter Vulnerabilität gezielt zu identifizieren und engmaschiger zu überwachen.
Keypoints
-
Hypertrophe Kardiomyopathie ist häufig mit diastolischer Dysfunktion und chronischer Vorhofbelastung assoziiert; der linke Vorhof ist funktionell früh mitbetroffen.
-
Vorhofflimmern stellt bei Patient:innen mit HCM einen klinischen Wendepunkt dar und ist mit abruptem Funktionsverlust, Hospitalisationsrisiko und erhöhter Thromboemboliegefahr verbunden.
-
Der „Left atrial strain“ (Reservoir-, Conduit- und Kontraktionsphase) liefert eine quantitative, funktionelle Beurteilung des linken Vorhofs über den Herzzyklus hinweg und geht über rein volumetrische Messgrößen hinaus.
-
In der HCM-Ambulanz am AKH Wien wird der LA Strain zur Risikostratifikation eingesetzt, um Patient:innen mit erhöhter Vulnerabilität für Vorhofflimmern frühzeitig zu identifizieren und engmaschig nachzuverfolgen.
Definition und klinische Einordnung der hypertrophen Kardiomyopathie
Die HCM ist definiert als Verdickung des (meist) linksventrikulären Myokards von ≥15mm, ohne dass alternative Ursachen wie arterielle Hypertonie oder relevante Klappenvitien vorliegen. In den meisten Fällen zeigt sich eine asymmetrische Septumhypertrophie; daneben existieren auch apikale und gemischt-hypertrophe Phänotypen. Bei einem wesentlichen Anteil der Betroffenen besteht eine genetische Mutation im Hintergrund, die einem autosomal dominanten Erbgang folgt. Aus klinischer Sicht unterscheidet man zwei funktionell relevante Erscheinungsformen:
Obstruktive HCM (HOCM)
Durch die Kombination aus septaler Hypertrophie und „systolic anterior motion“ (SAM) des Mitralsegels entsteht ein dynamischer Druckgradient im linksventrikulären Ausflusstrakt (LVOT). Dieser Gradientenanstieg führt zu einem limitierten Auswurf in der Systole, zu erhöhter intraventrikulärer Druckbelastung und sekundär zu einer funktionellen Mitralklappeninsuffizienz.
Nichtobstruktive HCM
Hier steht keine relevante LVOT-Obstruktion im Vordergrund, jedoch ist die diastolische Dysfunktion häufig stark ausgeprägt. Das hypertrophe, rigide Myokard füllt sich nur unter erhöhten enddiastolischen Drücken.
Symptomatik
In beiden Formen – obstruktiv und nichtobstruktiv – ist die Störung der diastolischen Füllung ein zentrales Problem. Typische Beschwerden umfassen:
-
Belastungsdyspnoe bereits bei geringer Aktivität
-
thorakalen Druck bzw. Beklemmungsgefühl
-
Palpitationen bzw. Episoden von Herzrasen
-
deutlichen Leistungsabfall im Alltag
-
Schwindel bis hin zu Präsynkopen/Synkopen
Der linke Vorhof bei HCM
Bei Patient:innen mit HCM ist der linke Vorhof in der Regel chronisch hämodynamisch belastet. Dafür sind mehrere Mechanismen verantwortlich.
Diastolische Dysfunktion
Das hypertrophe und wenig elastische Myokard füllt sich erschwert. Um ein ausreichendes enddiastolisches Volumen zu erreichen, benötigt der linke Ventrikel erhöhte Füllungsdrücke. Diese Druckerhöhung überträgt sich retrograd in den linken Vorhof. Der Vorhof muss somit dauerhaft gegen erhöhte Drücke arbeiten.
Obstruktion und Volumenbelastung
Bei der obstruktiven Form der HCM entsteht ein dynamischer LVOT-Gradient. Dieser führt in der Systole zu einem erhöhten intraventrikulären Druck und fördert eine systolische anterior gerichtete Mitralklappenbewegung (SAM). Das SAM-Phänomen verursacht häufig eine funktionelle Mitralklappeninsuffizienz. Regurgitierendes Blutvolumen gelangt systolisch in den linken Vorhof zurück.
Das bedeutet: Zusätzlich zur Druckbelastung durch die Störung der diastolischen Füllung kommt es zu einer Volumenbelastung des linken Vorhofs. Dieser Effekt ist bei der obstruktiven HCM typischerweise stärker ausgeprägt als bei der nichtobstruktiven Form.
Strukturelles Remodeling
Die chronische Druck- und Volumenbelastung führt zu einer linksatrialen Dilatation, zur Ausbildung von interstitieller Fibrose und zu elektrischer Heterogenität des Vorhofmyokards. Diese Umbauvorgänge bilden den Boden für atriale Arrhythmien bis hin zu persistierendem Vorhofflimmern.
Vorhofflimmern bei HCM – klinische Relevanz
Vorhofflimmern hat bei HCM eine deutlich größere hämodynamische Relevanz als bei strukturell normalen Herzen. Der Verlust der geordneten Vorhofkontraktion in der späten Diastole eliminiert den „atrial kick“, der bei Patient:innen mit restriktiver Füllungsphysiologie essenziell für die enddiastolische Volumenbereitstellung ist. Das Schlagvolumen sinkt unmittelbar, die Leistungslimitierung wird abrupt spürbar.
Bei obstruktiver HCM entsteht darüber hinaus ein Rückkopplungseffekt:
Reduzierte Vorhofkontraktion
→ verminderte LV-Füllung
→ kleineres enddiastolisches LV-Kavum
→ Zunahme des LVOT-Gradienten
→weiterer Abfall des effektiven Auswurfs
Klinisch resultieren daraus häufig eine progrediente Dyspnoe bis hin zur Orthopnoe, Kreislaufinstabilität unter Belastung sowie ein deutlicher Bedarf an interventioneller oder zumindest engmaschiger rhythmologischer Betreuung. Neben den hämodynamischen Konsequenzen ist das embolische Risiko von Vorhofflimmern (VHF) bei HCM hoch. Schon paroxysmales VHF gilt in diesem Kollektiv als Indikation zur Antikoagulation, auch bei niedrigen CHA2DS2-VA-Scores, da die Kombination aus atrialer Fibrose, Dilatation und Stase ein strukturell hohes Thromboembolierisiko birgt.
„Left atrial strain“: Methodik und klinische Bedeutung
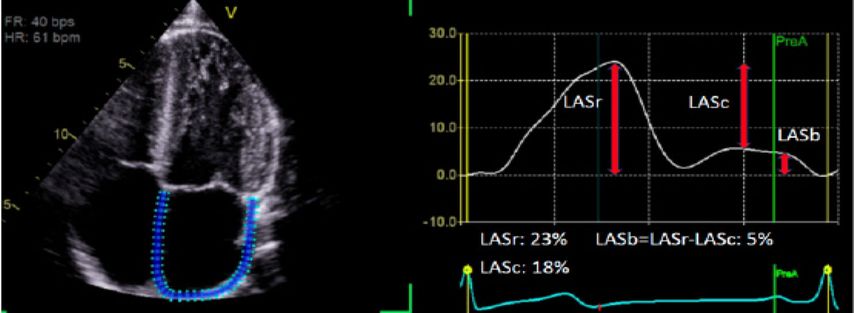
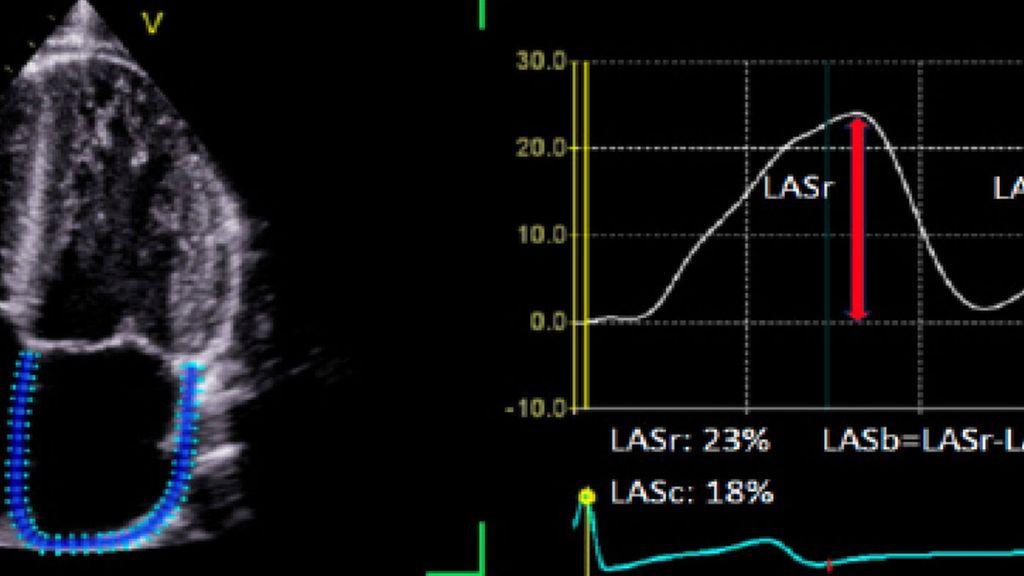
Die Analyse des „left atrial strain“ (LA Strain) basiert auf der „speckle-tracking“ Echokardiografie. Dabei werden standardisierte Echoaufnahmen des linken Vorhofs softwaregestützt ausgewertet. Die Methode verfolgt die Deformationsbewegung des Vorhofmyokards über den Herzzyklus hinweg. Aus dieser Bewegung werden prozentuale Längenänderungen („strain“) berechnet. Entscheidend ist, dass der „LA strain“ nicht nur die Größe des linken Vorhofs abbildet (wie etwa das linksatriale Volumen), sondern dessen funktionelle Leistungsfähigkeit. Drei Phasen werden üblicherweise unterschieden (Abb. 1):
Abb. 1: Abbildung eines LA Strain mit eingezeichnetem Strain. Abkürzungen: LASr = „Left atrial reservoir strain“ LASc = „Left atrial conduit strain“ LASb = „Left atrial booster strain“
„Reservoir strain“
Beschreibt die Fähigkeit des linken Vorhofs, sich während der Ventrikelsystole zu dehnen und Blut aus den Pulmonalvenen aufzunehmen. Eine eingeschränkte Reservoirfunktion spricht für verminderte Compliance und strukturelle Umbauvorgänge (Fibrose).
„Conduit strain“
Entspricht der passiven Weiterleitung des Bluts aus dem linken Vorhof in den linken Ventrikel in der frühen Diastole. Diese Phase reflektiert die Interaktion zwischen Vorhof und Ventrikel.
„Contraction strain“
Erfasst die aktive Kontraktion des linken Vorhofs in der späten Diastole („atrial kick“). Dieser Beitrag ist bei HCM-Patient:innen hämodynamisch bedeutsam. Eine eingeschränkte kontraktive Vorhoffunktion ist klinisch brisant, da genau dieser Mechanismus beim Auftreten von Vorhofflimmern wegfällt.
Die funktionelle Beeinträchtigung des linken Vorhofs kann bereits sichtbar gemacht werden, bevor es zur klinischen Manifestation von Vorhofflimmern kommt. Damit bietet der LA Strain einen zusätzlichen Baustein zur Risikostratifizierung.
Praxistipp
Bei Patient:innen mit HCM, die über neu aufgetretene Belastungsdyspnoe, Palpitationen oder abrupten Leistungsabfall berichten – auch ohne bereits dokumentiertes Vorhofflimmern im EKG –, sollte eine „speckle-tracking“-basierte Analyse des linken Vorhofs inklusive LA Strain durchgeführt werden. Ein eingeschränkter LA Strain ist als Frühwarnsignal für Rhythmusinstabilität zu werten und sollte zu enger rhythmologischer Überwachung (z.B. Holter/Event-Recorder) und frühzeitiger therapeutischer Planung führen.
Zusammenfassung
Die HCM ist eine strukturelle Herzerkrankung mit ausgeprägter diastolischer Komponente, wobei der linke Vorhof eine zentrale Funktion einnimmt. Vorhofflimmern markiert häufig einen klinisch relevanten Einschnitt und ist bei HCM mit deutlicher Zunahme der Symptomlast, reduzierter Belastbarkeit und erhöhtem Embolierisiko assoziiert. Der LA Strain erlaubt eine differenzierte, phasenweise Beurteilung der Vorhoffunktion (Reservoir, Conduit, Kontraktion) und ergänzt damit die klassische Echokardiografie um prognostisch relevante Informationen. In der klinischen Routine kann die Analyse des LA Strain dazu beitragen, Patient:innen mit erhöhtem Risiko für Vorhofflimmern frühzeitig zu erkennen und engmaschiger rhythmologisch zu betreuen.
Literatur:
bei den Verfassern
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...