Medikamenteninteraktionen: hochrelevant im klinischen Alltag
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei gleichzeitiger Einnahme mehrerer Medikamente ist die Wahrscheinlichkeit hoch, dass diese einander beeinflussen. Diese Wechselwirkungen können zum kompletten Wirkungsverlust oder auch zur Medikamentenvergiftung führen. Eine einfache Maßnahme besteht darin, Polypharmazie so gut wie möglich zu vermeiden.
Der wichtigste Risikofaktor für Medikamentenwechselwirkungen ist die Anzahl der Medikamente, so Univ.-Prof. Dr. Michael Wolzt, Universitätsklinik fürKlinische Pharmakologie am AKH Wien: „Nehmen Sie ein Medikament, kann kein anderes interagieren, nehmen Sie viele, gibt es viel Potenzial für Wechselwirkungen.“In den Fachinformationen ist das Interaktionspotenzial eines Medikaments unter Abschnitt 4.4 „Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung“ und Abschnitt 4.5 „Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen“ gelistet.
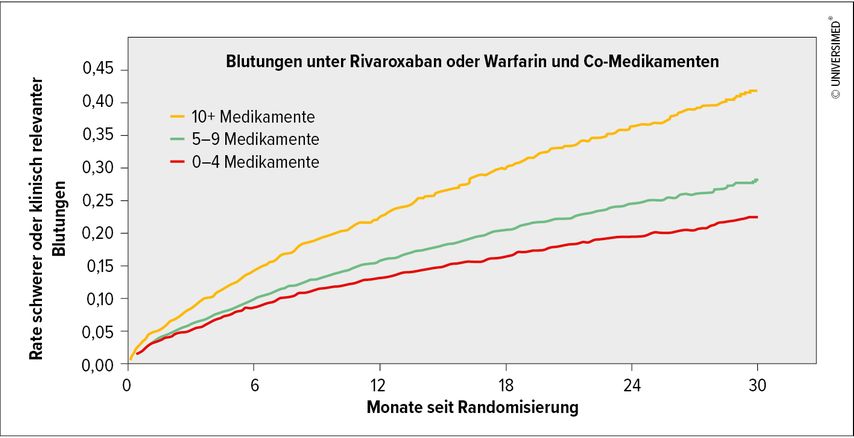
Eine häufige Manifestation von Arzneimittelinteraktionen ist ein erhöhtes Blutungsrisiko. Als Beispiel nannte Wolzt Blutungen unter Rivaroxaban oder Warfarin in Abhängigkeit von der Zahl der gleichzeitig eingenommenen Medikamente. So zeigen Analysen der Studie ROCKET AF, dass sich bei Einnahme von zehn oder mehr Medikamenten das Blutungsrisiko im Vergleich zu null bis vier eingenommenen Medikamenten verdoppelt. Dabei war es egal, um welcheAntikoagulation es sich handelte und welcheMedikamente im Spiel waren. Allein die Zahl steigerte das Risiko. Auch eine Normalisierung nach Risikoscores wie dem HAS-BLED änderte nichts an diesem Befund (Abb. 1).1
Abb. 1: Ergebnisse der Studie ROCKET AF zum Blutungsrisiko bei der Einnahme von Rivaroxaban oder Warfarin und weiteren Medikamenten (modifiziert nach Piccini JP et al. 2016)1
„Magenschutz“: keine Resorption bei zu wenig Magensäure
Das Nebenwirkungspotenzial beginnt im Magen. Für die Resorption müssen sich die Tabletten auflösen, die Salzbindung des Wirkstoffs muss gespalten werden. Vor allem bei schwachen Elektrolyten (milde Salze; Klasse II im biopharmazeutischen Klassifizierungssystem; BCS) ist dazu ein tiefer pH-Wert im Magen notwendig. Hemmer der Magensäure können daher die Dissolution der Arzneimittel beeinflussen.
Im biopharmazeutischen Klassifizierungssystem („Biopharmaceutics Classification System“) spielen die Begriffe Löslichkeit und Permeabilität eine wichtige Rolle, erläuterte Wolzt. Die Löslichkeit eines Arzneistoffes wird im BCS-System als hoch bewertet, wenn sich die höchste therapeutische Einzeldosis in 250ml Wasser über einen pH-Bereich von 1,2 bis 6,8 vollständig auflösen lässt – unabhängig vom Zeitfaktor. Die Permeabilität gibt an, wie gut ein Stoff die Magenbarriere durchdringt, eine gute Permeabilität entspricht einer Bioverfügbarkeit von ≥85%. Die Löslichkeit wird in vitroüberprüft. Die Überprüfung der Bioverfügbarkeit erfolgt durch den Vergleich der Plasmaspiegel nach oraler Einnahme und intravenöser Applikation. Wolzt: „Ist die Löslichkeit einer Tablette relativ schlecht, die Permeabilität jedoch gut, dann wird es vom pH-Wert im Magen abhängen, wie viel der Wirksubstanz Sie tatsächlich im Körper finden.“ Die Modellsubstanz für dieses Konzept ist das Schmerzmittel Ibuprofen. Mit Ibuprofen konnte nicht nur gezeigt werden, dass der pH-Wert im Magen entscheidend für die Löslichkeit ist, sondern dass auch das Lösungsmedium entscheidet. So zeigte sich eine schlechtere Löslichkeit, wenn Ibuprofen mit Fruchtsaft eingenommen wird, während gleichzeitiger Konsum von Alkohol die Löslichkeit eher verbessert.
Ein in der Praxis sehr relevantes Beispiel ist die Einnahme von Schilddrüsenhormon (Levothyroxin). Die Tabletten sollen morgens mit einem Glas Wasser eingenommen werden. Die optimale Löslichkeit der Tabletten wird bei einem sehr sauren Magen-pH-Wert von 1,2 erreicht. Bei höherem pH-Wert löst sich das Medikament schlecht und langsam.2
Wolzt: „Wenn sich bei Patienten keine entsprechende Wirkung einstellt, dann muss das nicht unbedingt auf mangelnde Adhärenz oder Nichtbefolgen des Abstandes zwischen Medikamenteneinnahme und Frühstück hindeuten. Es kann auch sein, dass das Milieu im Magen einfach nicht sauer genug ist, weil der Patient beispielsweise einen Protonenpumpen-Inhibitor einnimmt.“ Dies betrifft nicht nur Schilddrüsenhormon. Auch Berichte über eine Abnahme des Blutungsrisikos bei Kombination von Dabigatran mit einem Protonenpumpen-Inhibitor (PPI) gehen nicht ausschließlich darauf zurück, dass der PPI die Magenschleimhaut schützt, sondern auf eine schlechtere Resorption von direkten oralen Antikoagulanzien (DOAK) aufgrund eines höheren pH-Werts im Magen – womit auch die Wirksamkeit eingeschränkt ist.3 Wolzt: „Sie unterdosieren daher manchmal Ihre Patienten, indem Sie den Magen-pH-Wert durch PPI so weit anheben, dass sich die Tabletten nicht mehr auflösen können.“ Dies betrifft beispielsweise auch Vericiguat, den zur Behandlung von Erwachsenen mit dekompensierter Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF) zugelassenen sGC-Stimulator, bei dem „Magenschutz“ die Plasmaspiegel um bis zu 50% reduziert.4
Praxistipp: saure Getränke für die Medikamenteneinnahme
Reduzierte Aufnahme infolge eines zu hohen pH-Werts im Magen stellt auch bei Krebstherapien mit CDK4/6-Hemmern ein ernstes Problem dar. So werden mit Abemaciclib, Palbociclib und Ribociclib bei Brustkrebs konsistente und klinisch relevante Verlängerungen der progressionsfreien Überlebenszeit und des Gesamtüberlebens erreicht. Die Einnahme von PPI kann jedoch zum Wirkverlust der CDK4/6-Hemmer führen.5
Dieses Problem ist nicht nur im individuellen Fall, sondern auch auf Populationsebene relevant. So erhielten laut Daten der Österreichischen Gesundheitskasse (ÖGK) im 1. Halbjahr 2023 in Österreich 1982 Patient:innen einen CDK4/6-Inhibitor – 954 Palbociclib, 615 Abemaciclib und 466 Ribociclib. Wie viele davon PPI einnehmen, lässt sich nur schätzen, da die Kassenpreise mehrerer PPI unter der Rezeptgebühr liegen und es daher keine verlässlichen Daten über die ausgegebenen Mengen gibt.Eine Auswertung der Personen mit Gebührenbefreiung (Subgruppe) ergibt 60% PPI-Überlappung. Wolzt: „Das ist kein Randgruppen-Phänomen. Das bedeutet, dass 60% der Patient:innen nicht nur onkologische Medikamente im Wert von Tausenden Euro letztlich die Toilette hinunterspülen, sondern gleichzeitig auch deren Wirksamkeit auf null reduzieren. Das ist dramatisch.“
Die EMA hat nun die Hersteller von PPI aufgefordert, umfangreiche Sicherheitsdaten nachzuliefern und das Interaktionspotenzial zu erheben. Ein praktischer Ausweg liegt darin, die Medikamente zusammen mit sauren Flüssigkeiten einzunehmen. Dazu bietet sich beispielsweise „Coca-Cola classic“ mit einem pH-Wert von 2,5 an. Dass dies tatsächlich funktioniert, konnte am Beispiel des HIV-Medikaments Velpatasvir und des PPI Omeprazol demonstriert werden.6 Diese Strategie funktioniert auch bei einer Reihe von Antiinfektiva wie Cefditoren, Cefpodoxim, Cefuroxim, Itraconazol, Ketoconazol, Posaconazol, Atazanavir, Delavirdin, Emtricitabin/Rilpivirin/Tenofovir, Nelfinavir, Raltegravir, Ledipasvir/Sofosbuvir undSofosbuvir/Velpatasvir.
Achtung, Vergiftungsgefahr: Interaktionen am CYP P450
Wichtig für Medikamenteninteraktionen sind auch die ca. 60 Enzyme (Monooxygenasen) des Cytochrom-P450-Systems, die vor allem in Leber und Darmmukosa exprimiert werden. Dieses weist einerseits individuelle Besonderheiten durch genetische Alterationen auf („ultrarapid“, „extensive“, „intermediate“, „poor metabolizer“), kann andererseits aber auch durch Induktoren und Inhibitoren beeinflusst werden. Eine starke CYP-Inhibition erhöht die „area under the curve“ (AUC) mindestens fünffach oder reduziert die Clearance von Substraten um ≥80%. CYP-Inhibition führt also dazu, dass Substanzen, die über das betroffene Cytochrom metabolisiert werden, langsamer abgebaut werden und im Körper akkumulieren. Wolzt wies darauf hin, dass die Zusammenhänge meist noch deutlich komplexer sind, da kaum eine Substanz über einen einzigen Weg metabolisiert wird. Daher müssen Interaktionen am Cytochrom P450 in der Praxis in Tabellen nachgeschlagen oder mit entsprechenden Apps abgefragt werden.
Ein Beispiel dafür, wie man Interaktionen am Cytochrom P450 kreativ nützen kann, ist Ritonavir, das 1996 für die HIV-Therapie zugelassen und wenig später wegen schlechter Verträglichkeit wieder vom Markt genommen wurde. Ritonavir bewirkt eine irreversible CYP3A4-Hemmung (max. Effekt nach 48h, anhaltende Dauer über ca. drei Tage nach Beendigung) und kann daher als Booster für andere Medikamente genützt werden, da es deren biologische Halbwertzeit verlängert. Konkret macht man sich das beim Einsatz der HIV-Protease-Inhibitoren sowie von Nirmatrelvir zunutze. Dies kann allerdings zu erheblichen Problemen führen, wenn zusätzlich zu Ritonavir-geboosterten Medikamenten weitere Substanzen eingenommen werden, deren Abbau durch Ritonavir ebenfalls verzögert wird. Dies konnte beispielsweise für das DOAK Rivaroxaban gezeigt werden.7
Wolzt: „Mit einer Ritonavir-haltigen Therapie besteht die Gefahr, iatrogene Vergiftungen mit anderen Medikamenten zu erzeugen. Erst drei Tage nach Ritonavir-Gabe normalisiert sich der Leberstoffwechsel wieder. Werden andere Medikamente, die über CYP3A4 metabolisiert werden, wie gewohnt weiter eingenommen, so kann es zu dramatischen Anstiegen der Wirkstoffspiegel kommen. Daher sind entsprechende Therapieumstellungen unbedingt und rechtzeitig vorzunehmen.“ Den gegenteiligen Effekt haben CYP-Induktoren, die das Substrat entsprechend reduzieren können. Beispiele sind Carbamazepin (1A2, 3A4/5), Rifampicin (2C8, 3A4/5) und Enzalutamid (3A4/5).
Als Faustregel empfiehlt Wolzt, auf Medikamente mit geringer therapeutischer Breite zu achten undim Zweifel und Akutfall nichtessenzielle Arzneimittel (=prophylaktische Medikamente) zu pausieren, aber einen möglichen Rebound zu bedenken. BeiVersuch der Reduktion von Polymedikationgilt das Prinzip: Therapie vor Prophylaxe.
Quelle:
„Relevante Medikamenteninteraktionen“, Vortrag von Univ.-Prof. Dr. Michael Wolzt, Wien, am 12. April 2024 im Rahmen des ÖIK in Saalfelden
Literatur:
1 Piccini JP et al.: Circulation 2016; 133: 352-60 2 Dimple P et al.: Eur J Pharm Biopharm 2009; 72(1): 105-10 3 Bolek T et al.: Semin Thromb Hemost 2019; 45(8): 846-50 4 Fritsch A et al.: Clin Pharmacokinet 2024; 63(6): 751-71 5 Lee JE et al.: JAMA Netw Open 2023; 6(7): e2324852 6 Van Seyen M et al.: Clin Pharmacol Ther 2019; 106(5): 1093-8 7 Weinz C et al.: Drug Metab Dispos 2009; 37(5): 1056-64
Das könnte Sie auch interessieren:
Infektionen in der Schwangerschaft: Zikavirus, Parvovirus, CMV & Co
Das Thema viraler Schwangerschaftsinfektionen präsentiert sich wie ein Eisberg, so Assoc. Prof. Priv.-Doz. Dr. Lukas Weseslindtner, Zentrum für Virologie der Medizinischen Universität ...
Mit Antikörpern gegen bakterielle Infektionen
In Zeiten zunehmender Antibiotikaresistenzen werden innovative Strategien gegen bakterielle Erreger dringend benötigt. Als eine der potenziellen Lösungen bieten sich therapeutische ...
Infektionen in Krankenhäusern in Deutschland
Welche Infektionen führen häufig zu Hospitalisierungen und wie viel kostet die stationäre Behandlung von Infektionskrankheiten? Eine deutsche Expert:innengruppe versuchte, diese Fragen ...