Timing der Operation im Rahmen der Primärtherapie
Autor:
Assoz. Prof. Priv.-Doz. Dr. Christoph Grimm
Klinische Abteilung für Allgemeine Gynäkologie und Gynäkologische Onkologie
Universitätsklinik für Frauenheilkunde Medizinische Universität Wien
E-Mail: christoph.grimm@meduniwien.ac.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Auch in der Ära zielgerichteter Therapien bleibt der postoperative Tumorrest einer der wichtigsten prognostischen Faktoren beim fortgeschrittenen Ovarialkarzinom. Frühere Studien zum optimalen Operationszeitpunkt (Primär- vs. Intervall-Debulking) litten unter methodischen Schwächen und eingeschränkter operativer Qualität. Mit der TRUST-Studie liegt nun erstmals eine qualitativ hochwertige Untersuchung zu dieser klinisch hochrelevanten Fragestellung vor.
Stellenwert der Debulkingoperation inkl. HIPEC
Der postoperative Tumorrest – sowohl nach primärer Debulkingoperation (PDS) als auch nach Intervall-Debulkingoperation (IDS) – ist einer der wichtigsten prognostischen Parameter für den Krankheitsverlauf bei fortgeschrittenem Ovarialkarzinom. Diese Relevanz wurde auch in der Ära zielgerichteter Therapien und prädiktiver Biomarker bestätigt.1 Eine prophylaktische systematische Lymphadenektomie unauffälliger Lymphknoten zeigte hingegen keinen prognostischen Vorteil.2 Somit kann ein unnötiger Operationsschritt vermieden und perioperative Morbidität reduziert werden.
Die hypertherme intraperitoneale Chemotherapie (HIPEC) ist derzeit keine Standardtherapie und sollte ausschließlich in prospektiven kontrollierten Studien eingesetzt werden. Während van Driel et al. (2018)3 einen Überlebensvorteil durch HIPEC zeigten, konnten Lim et al. (2022)4 keinen signifikanten Unterschied für das progressionsfreie oder Gesamtüberleben nachweisen. Aufgrund der erhöhten Morbidität und der heterogenen Datenlage sollte HIPEC weiterhin nur im Rahmen klinischer Studien angewendet werden.
Bisherige Datenlage zum Timing der Debulkingoperation
Zwei randomisierte Studien, die EORTC-Studie5 und die CHORUS-Studie6,zeigten ein vergleichbares Gesamtüberleben für PDS und IDS. Beide Studien litten jedoch unter Limitationen wie niedrigen Raten an Komplettresektionen (25% bzw. 40%), kurzen Operationszeiten und einem hohen Anteil an Patientinnen mit schlechtem Allgemeinzustand. Diese Einschränkungen führten zu einer kontroversen Diskussion über die optimale Vorgehensweise und waren Anlass für die Durchführung der TRUST-Studie.
Neue Erkenntnisse durch die TRUST-Studie
In die TRUST-Studie7 wurden 796 Patientinnen mit fortgeschrittenem epithelialem Ovarialkarzinom im Stadium FIGO ≥IIB eingeschlossen und randomisiert einer PDS- oder IDS-Gruppe zugeteilt.Die TRUST-Studie zeichnete sich durch eine rigorose Qualitätskontrolle der operativen Expertise der teilnehmenden Zentren aus (unter anderem Live-Operation, Begutachtung der Operationsprotokolle, konsekutive Begutachtung der Patientinnenströme der letzten 3 Jahre vor Studienbeginn). Der primäre Endpunkt war das Gesamtüberleben (OS), sekundäre Endpunkte waren das progressionsfreie Überleben (PFS) sowie die perioperativen Komplikationen.
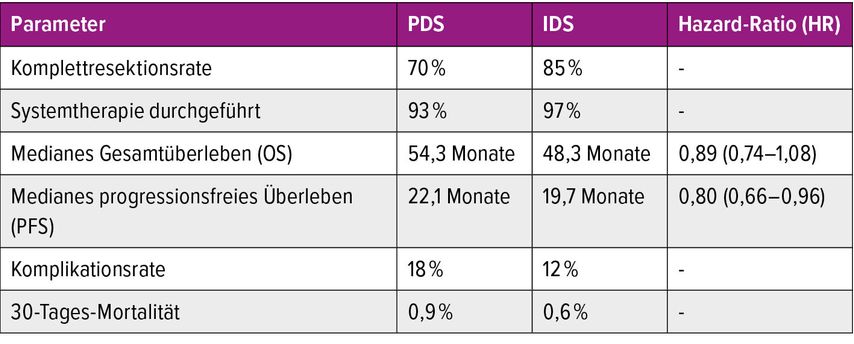
Die Komplettresektionsrate lag in der PDS-Gruppe bei 70% und in der IDS-Gruppe bei 85%. Die Systemtherapie konnte bei 93% (PDS) bzw. 97% (IDS) durchgeführt werden. Das mediane OS betrug 54,3 Monate (PDS) versus 48,3 Monate (IDS), HR: 0,89 (95%CI: 0,74–1,08). Das mediane PFS lag bei 22,1 Monaten (PDS) versus 19,7 Monate (IDS), HR: 0,80 (95%CI: 0,66–0,96). Die Komplikationsraten waren vergleichbar: 18% (PDS) versus 12% (IDS). Die 30-Tages-Mortalität lag unter 1% in beiden Gruppen (Tab. 1.).
Tab. 1: Vergleich der Ergebnisse von PDS vs. IDS in der TRUST-Studie. Die TRUST-Studie zeigte keinen signifikanten Unterschied im Gesamtüberleben zwischen PDS und IDS, jedoch einen Vorteil im progressionsfreien Überleben zugunsten von PDS
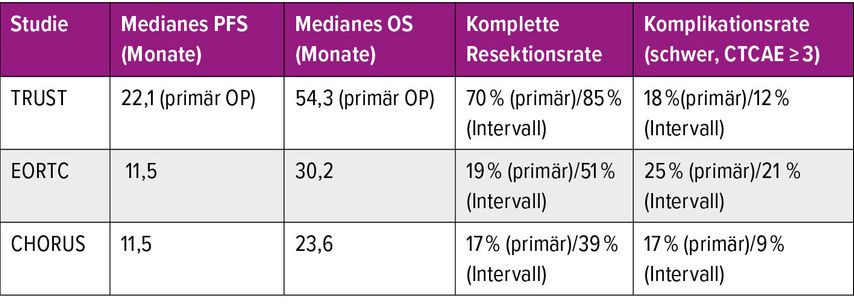
Im Vergleich zu den bisherigen Studien unterscheidet sich die TRUST-Studie bezüglich der Komplettresektionsrate beträchtlich (Tab. 2.). Dies führt zu einem deutlich längeren progressionsfreien und Gesamtüberleben. Erfreulicherweise kann diese bessere Prognose trotz ausgedehnterer Operation mit vergleichbarer bis niedrigerer Komplikationsrate erreicht werden (Tab. 2.). Die TRUST-Studie zeigt, dass kein signifikanter Überlebensvorteil für PDS gegenüber IDS besteht. Sie ist jedoch die erste randomisierte Studie, die einen Vorteil im progressionsfreien Überleben für PDS belegt. Diese Ergebnisse unterstreichen die Bedeutung der Patientinnenselektion: Insbesondere Patientinnen mit gutem Allgemeinzustand und günstiger intraabdominaler Tumorverteilung können von einer primären Debulkingoperation profitieren. Aufgrund der Komplexität des Eingriffs sollte die Durchführung einer solchen Operation in hochspezialisierten Zentren mit hoher chirurgischer Expertise erfolgen.
Tab. 2: Vergleich der CHORUS-, EORTC- und TRUST-Studie bezüglich Wirksamkeit und Komplikationsraten. CTCAE = „criteria for adverse events“
Fazit
Die TRUST-Studie liefert erstmals qualitativ hochwertige Daten, die die Diskussion über das optimale Timing der Operation beim fortgeschrittenen Ovarialkarzinom entscheidend bereichern. Während das Gesamtüberleben vergleichbar ist, zeigt sich ein längeres progressionsfreies Überleben nach PDS.Diese Studie belegt, dass durch die Durchführung dieser komplexen Operation in hochspezialisierte Zentren mit entsprechender fachlicher und operativer Expertise die Prognose der Patientinnen entscheidend verbessert werden kann, und unterstreicht die Bedeutung der Zentralisierung dieser Eingriffe.
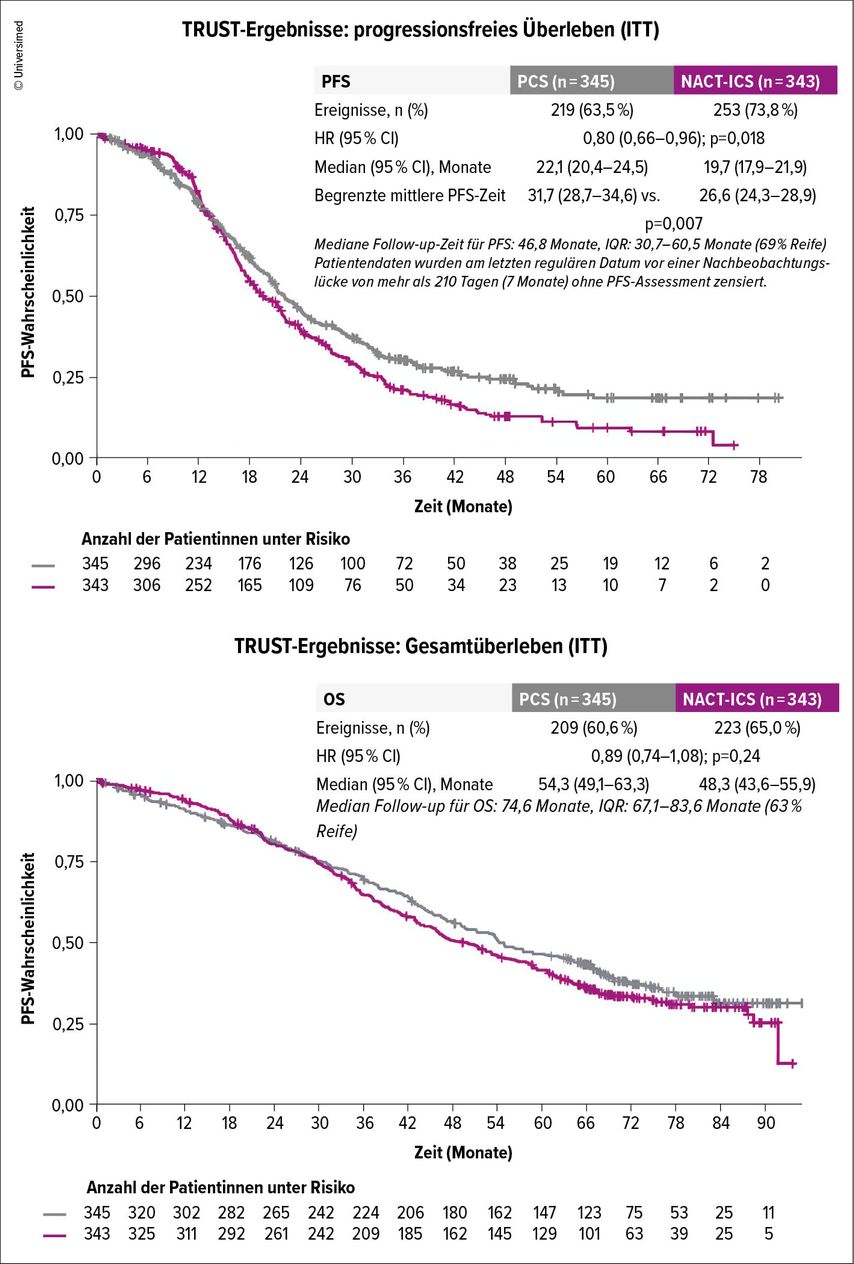
Abb. 1: Progressionsfreies Überleben und Gesamtüberleben von Patientinnen mit fortgeschrittenem Ovarialkarzinom nach PDS und IDS im Rahmen der TRUST-Studie (beide Abbildungen modifiziert nach der Präsentation von Prof. Sven Mahner vom ASCO 2025)
Literatur:
1 Ray-Coquard I et al.: Olaparib plus bevacizumab as first-line maintenance in ovarian cancer (PAOLA-1). N Engl J Med 2019; 381(25): 2416-28 2 Harter P et al.: Lymphadenectomy in ovarian neoplasms (LION): a randomised, phase 3 trial. N Engl J Med 2019; 380(9): 822-32 3 van Driel WJ et al.: Hyperthermic intraperitoneal chemotherapy in ovarian cancer. N Engl J Med 2018; 378(14): 230-40 4 Lim MC et al.: Randomized trial of hyperthermic intraperitoneal chemotherapy (HIPEC) in women with primary advanced peritoneal, ovarian, and tubal cancer. J Clin Oncol 2022; 40(3): 267-76 5 Vergote I et al.: Neoadjuvant chemotherapy or primary surgery in stage IIIC or IV ovarian cancer. N Engl J Med 2010; 363(10): 943-53 6 Kehoe S et al.: Primary chemotherapy versus primary surgery for newly diagnosed advanced ovarian cancer (CHORUS): an open-label, randomised, controlled, non-inferiority trial. Lancet 2015; 386(9990): 249-57 7 Mahner S et al.: TRUST (ENGOT-ov33): A randomized phase III trial comparing primary vs interval debulking surgery in advanced ovarian cancer. J Clin Oncol 2023; 41(suppl): LBA5500
Das könnte Sie auch interessieren:
Unser Universimed-Team berichtet für Sie aus Salzburg!
Die Jahrestagung der OEGGG findet in diesem Jahr vom 30. Mai bis 2. Juni in Salzburg statt. Diese Veranstaltung ist zweifelsohne eine der bedeutendsten Tagungen für Gynäkologinnen und ...
OeGGG 2018
...
OeGGG 2018
Test...