Die Rolle von Lifestylefaktoren in der Vor- und Nachsorge
Autorinnen:
Dr.med. Karin Breu
Dr.med. Natalie Gabriel
Frauenklinik Stadtspital Zürich
E-Mail: natalie.gabriel@stadtspital.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Anzahl der Langzeitüberlebenden nach Krebserkrankungen steigt seit mehreren Jahrzehnten kontinuierlich. Die psychosozialen und medizinischen Bedürfnisse von Krebsüberlebenden finden zunehmend Beachtung in der Forschung und in der klinischen Tätigkeit. Die Förderung eines gesunden Verhaltens mit Erfassung und Beratung hinsichtlich Ernährung, Nikotinabstinenz, Alkoholkonsumreduktion, Gewichtskontrolle, körperlicher Aktivität sowie Stressreduktion spielt in der Betreuung von Krebspatientinnen, aber auch generell in der Krebsvorsorge eine wichtige Rolle. Gewichtsabnahme bei vorbestehender Adipositas und regelmässige körperliche Aktivität wirken sich positiv auf die Lebensqualität, aber auch auf die krebsassoziierte Mortalität aus. Ähnlich der individualisierten Therapie sollten auch die Vorsorge und Nachbetreuung individualisiert werden.
Keypoints
-
Rauchen vermeiden: Ein Rauchstopp senkt das Krebsrisiko erheblich und verbessert die Behandlungsergebnisse. Rauchen in der Adoleszenz ist mit einem deutlich erhöhten Risiko für die Entwicklung eines späteren Mammakarzinoms assoziiert.
-
Bei Status nach Mammakarzinom sollte nach Möglichkeit ganz auf Alkohol verzichtet werden oder zumindest der regelmässige Konsum auf ein Minimum reduziert werden.
-
Eine Gewichtsreduktion bei Adipositas bzw. eine Reduktion des Fettgewebeanteils führt zu einem besseren onkologischen Outcome.
-
Bewegung fördern: Regelmässige körperliche Aktivität erhöht die Lebensqualität, reduziert die Sterblichkeit und sollte mindestens 150 Minuten moderate oder 75 Minuten intensive Bewegung pro Woche umfassen.
-
Nachsorge mit dem Fokus auf individuelle Lifestyleberatung
Neben den wenigen evidenzbasierten klinischen Untersuchungen kann die individuelle Beratung hinsichtlich Lifestylefaktoren in der Tumornachbehandlung einen grossen Benefit für die Patientin bieten. In der Folge werden wir auf die modulierbaren Lifestylefaktoren Ernährung, Bewegung, Nikotin und Alkohol eingehen.
Nikotin
Einfluss vor der Krebsdiagnose
Zahlreiche Studien haben den Zusammenhang zwischen Rauchen und verschiedenen Krebserkrankungen untersucht. Insgesamt ist Rauchen der bedeutendste vermeidbare Risikofaktor für die Entstehung von Krebs. Ein Rauchstopp reduziert das Risiko von 12 verschiedenen Krebsarten, wobei im Bereich der Frauenheilkunde eine Assoziation mit dem Mammakarzinom und dem Zervixkarzinom postuliert wird. Ein besonderes Interesse gilt dem möglichen Einfluss von Nikotin bzw. Tabakkonsum auf das Risiko für Brustkrebs.
Untersuchungen zeigen, dass Frauen, die jemals geraucht haben, ein um 14% höheres Risiko für Brustkrebs aufweisen als Nichtraucherinnen. Das relative Risiko steigt auf 35%, wenn eine positive Familienanamnese für Brustkrebs vorliegt. Vor allem das Rauchen in der Adoleszenz ist ein grosser und relevanter Risikofaktor für die Entstehung eines Mammakarzinoms zu einem späteren Zeitpunkt im Leben.
Frauen, die vor dem 17. Lebensjahr mit dem Rauchen begonnen haben, haben ein erhöhtes relatives Risiko von 24%. Neben der Dauer des Nikotinkonsums ist auch der Zeitpunkt des Rauchbeginns von Bedeutung.Der Zeitraum von der Menarche bis zur ersten ausgetragenen Schwangerschaft ist kritisch. Bis zur vollständigen Differenzierungdes Brustgewebes nach der Geburt des ersten Kindes ist das Brustgewebe am anfälligsten für krebserregende Einflüsse des Rauchens. Bei einer Dauer von zehn Jahren steigt das Risiko im Vergleich zu Nichtraucherinnen relevant auf 60%, was einem relativen Risiko von Langzeitraucherinnen, die über 40 Jahre hinweg rauchten, entspricht.
Beratung während der Behandlung und in der Nachsorge
Die Rate der Raucher nach kurativer Therapie einer Krebserkrankung unterscheidet sich je nach Krebsdiagnose stark. Eine niedrige Rate findet sich bei Frauen nach Brustkrebs (9,4%). Klar höher ist diese bei Frauen nach Uteruskarzinom mit 27,1% bzw. bei einem Zervixkarzinom mit 41%. Von den Patientinnen, die vorübergehend auf das Rauchen verzichten konnten, wird ein Drittel wieder rückfällig. Besonders häufig tritt dieser Rückfall bei Frauen mit Zervixkarzinom auf.
Rauchen ist bei einer Krebsdiagnose grundsätzlich mit einer erhöhten Mortalität verbunden. Dies ist multifaktoriell bedingt. Ein Rauchstopp verbessert die Ergebnisse der Krebsbehandlung, da ein persistierender Zigarettenkonsum diverse Auswirkungen auf die onkologische Therapie hat und zu vermehrten therapiebedingten Komplikationen führt. Zusätzlich wird mit einem Rauchstopp das Risiko für die Entwicklung einer zweiten tabakassoziierten Krebserkrankung bzw. für weitere nikotinbedingte Erkrankungen vermindert. Bei einer Radiotherapie erhöht sich bei Raucherinnen das relative Risiko für Sekundärkarzinome um bis zu 80%. Mehrere Studien weisen darauf hin, dass Raucherinnen ein erhöhtes relatives Risiko für ein Rezidiv haben. So erhöht sich bei Brustkrebspatientinnen mit persistierendem Nikotinabusus das Risiko für ein Spätrezidiv um 30% bis 41%. Wird der Zigarettenkonsum nach der Brustkrebsdiagnose nicht eingestellt, kann dies zu einer Erhöhung der Mortalität um bis zu 60% führen.
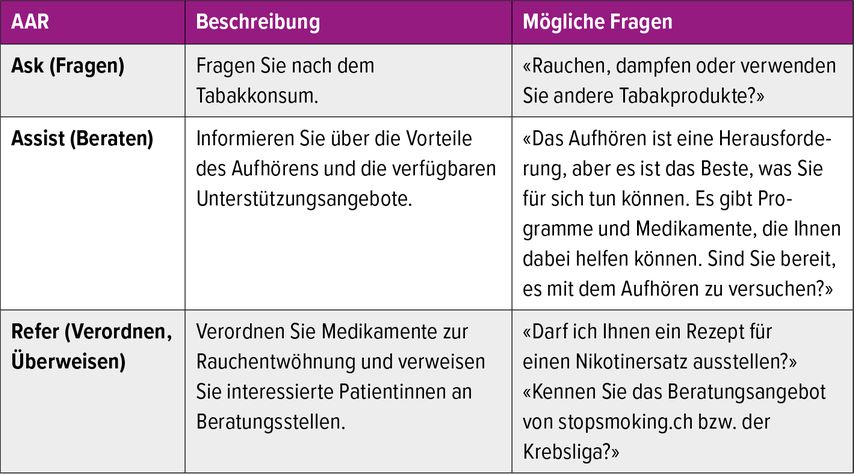
Eine Krebsdiagnose kann grundsätzlich die Motivation zum Rauchstopp erhöhen. Die behandelnde Fachperson spielt dabei eine entscheidende Rolle, indem sie die Bereitschaft der Patientin, mit dem Rauchen aufzuhören, direkt nutzen kann. Bereits eine kurze Beratung bei der Erstkonsultation erweist sich als effektiv. Massnahmen zur Förderung des frühzeitigen Rauchstopps, also vor Beginn der multimodalen onkologischen Therapie, kann die langfristige Rauchabstinenz bei Krebspatientinnen begünstigen. Ebenso erhöht ein während der onkologischen Therapie integriertes Nichtraucherprogramm nachhaltig die Erfolgsrate des Rauchstopps (Tab. 1)
Tab. 1: AAR: «Ask, assist, refer» (modifiziert nach Empfehlung der American Lung Association: Tobacco cessation quick reference guide)
Alkoholkonsum
Alkoholkonsum spielt nicht nur in der Entstehung von Karzinomen des Ösophagus und der Leber eine wesentliche Rolle, sondern ebenfalls bei vielen weiteren Krebsarten wie Brust-, Kolon- und Rektum- sowie Mundhöhlen- und Pharynxkarzinomen. Brustkrebs ist die dritthäufigste durch Alkoholkonsum verursachte Krebserkrankung. In der Entstehung von Brustkrebs scheint der Alkoholkonsum von den beeinflussbaren Faktoren das höchste Risiko zu haben.
Alkohol wirkt als direkter Tumorpromotor durch Zellschädigung wie Störung der DNA-Methylierung und der Reparationsmechanismen während des Alkoholabbauprozesses von Ethanol zu Acetaldehyd sowie der Bildung von freien Radikalen. Alkohol erhöht den Spiegel des zirkulierenden Östrogens, was insbesondere bei Entstehung von Mammakarzinomen und Endometriumkarzinomen eine Rolle spielt. In Kombination mit Nikotinabusus kumuliert sich das Risiko für Zellschäden durch Toxine. Frauen sind anfälliger für Nebenwirkungen des Alkoholkonsums als Männer und tolerieren eine niedrigere Alkohlmenge. Letztendlich hat aber jede konsumierte Alkoholmenge ein potenzielles Risiko.
Einfluss vor der Krebsdiagnose
Die Korrelation zwischen Alkoholkonsum und Entstehung von Brustkrebs ist schwierig validierbar aufgrund der Unzuverlässigkeit der Deklaration der konsumierten Menge und der Definition eines repräsentativen Kontrollarms. Es ist jedoch klar erwiesen, dass das Risiko, an einem Brustkrebs zu erkranken, 25–30% höher bei übermässigem Alkoholkonsum ist, wobei dieser vorallem die Entstehung von Östrogenrezeptor-positiven Mammakarzinomen begünstigt. Die Grenze der schädlichen Alkoholmenge für Frauen wird bei 10g Alkohol/Tag definiert. Dies entspricht jeweils einem Glas Wein, einer Stange Bier oder 0,3dl hochprozentigem Alkohol in einem Cocktail pro Tag. Das relative Risiko, an Brustkrebs zu erkranken, steigt um 9–13% pro jede weiteren 10g Alkoholkonsum pro Tag.
Beratung in der Nachsorge
Wie zu erwarten, führt das Weiterführen eines regelmässigen Alkoholkonsums nach stattgefundener Krebserkrankung zu einem schlechteren Outcome, wobei die tolerierbare, empfohlene Alkoholkonsummenge noch niedriger ist. Bei einer Alkoholkonsummenge von mehr als 10g pro Tag ist das relative Risiko für eine Metastasierung oder lokales Wiederauftreten bei Brustkrebs als Rezidiv oder Zweitkarzinom um 35% erhöht. Das relative Risiko, an Brustkrebs zu sterben, ist um 51% erhöht und wird nicht durch den postulierten kardioprotektiven Effekt kompensiert. Betroffen von diesem negativen Effekt scheinen vorallem postmenopausale und übergewichtige Mammakarzinompatientinnen mit Östrogenrezeptor-positiven Tumoren zu sein.
Die Aufklärung in der Nachsorge über die Gefahr des regelmässigen Alkoholkonsums auf das onkologische Outcome sollte ein wesentlicher Bestandteil sein. Der Patientin wird empfohlen, ganz auf Alkoholkonsum zu verzichten bzw. die maximale Menge auf weniger als 5g pro Tag zu reduzieren, was im Durchschnitt drei Drinks bzw. Gläser pro Woche entsprechen würde.
Adipositas
Auch in Europa ist die Prävalenz der Adipositas stetig steigend. Gemäss World Obesity Atlas wird erwartet, dass bis ins Jahr 2030 30% aller Männer und Frauen einen BMI >30kg/m2 haben werden. Epidemiologische Studien zeigen eine deutliche Assoziation zwischen Adipositas und einem erhöhten Risiko für die Entwicklung verschiedener Karzinome. Dabei sind die Krebsarten wie Ösophaguskarzinom, Gallenblasenkarzinom und Endometriumkarzinom bei der Frau mit dem höchsten relativen Risiko verbunden, gefolgt vonNierenzellkarzinom, Mammakarzinom und Pankreaskarzinom.
Die Entstehung und das Wachstum von Krebszellen ist insbesondere bei hormonabhängigen Karzinomen durch die gesteigerte Östrogenbildung bei vermehrter Expression von Aromatase in den Adipozyten erklärbar. Ein indirekter Effekt erfolgt durch die Adipositas-bedingte chronische Inflammation durch von im Fettgewebe synthetisierte Zytokine und vermehrter Synthese adipogener Wachstumsfaktoren wie Leptin. Ein weiterer kausaler Faktor sind die im Rahmen des metabolischen Syndroms erhöhten Insulinspiegel. Insulin reguliert nebst der Glukosehomöostase auch wichtige Wachstumsfaktoren wie «insulin-like growth factor» (IGF-1) bzw. stimuliert Tumorzellwachstum direkt via Insulinrezeptoren.
Beratung in der Nachsorge
Für Brustkrebspatientinnen gibt es einen klaren Zusammenhang zwischen Übergewicht und schlechterer Prognose zum Zeitpunkt der Diagnose, während der Behandlung und in der Nachsorge sowohl für Lokalrezidive, Fernmetastasierung, Brustkrebsmortalität und Zweitkarzinom. Das Risiko steigt bereits ab einem BMI >25kg/m2 und nimmt linear mit steigendem BMI zu. So ist z.B. das relative Sterberisiko bei Brustkrebs bei einem BMI >30 um 20–40% höher als bei Normalgewichtigen. Auf die Wirksamkeit der onkologischen Therapien scheint die Höhe des BMI jedoch keinen Einfluss zu haben.
Jedoch ist auch bei normalem BMI ein hoher Körperfettanteil mit einem schlechteren onkologischen Outcome assoziiert.
Mediterrane Ernährung mit reichlich Olivenöl extra vergine (≥15% der täglichen Energiezufuhr) mit vermehrtem Gemüse-/Früchtekonsum (v.a. Zitrusfrüchte), ballaststoffreiche, fettarme Vollwertkost wird als diätetische Massnahme empfohlen. Dabei sollte ausser dem Olivenöl extra vergine auf eine fettarme Ernährung geachtet werden. Eine Auswertung der Nurses’ Health Study II zeigte, dass ein Ernährungsmuster im Sinne einer «western diet» in der Adoleszenz bzw. im frühen Erwachsenenalter das Risiko für ein prämenopausales Mammakarzinom deutlich erhöht. Hierzu zählen zuckerhaltige Getränke, raffinierter Zucker und Getreide (Weissbrot, Bagel, Brötchen, Kekse, Reis, Nudeln, Pfannkuchen etc.), rotes Fleisch, verarbeitetes Fleisch und Fleischprodukte, gesättigte Fette, Margarine, Thunfisch, Makrele, Sardinen.
Insgesamt ist jedoch ein positiver Effekt auf das Brustkrebsrisiko nur nachweisbar, wenn bei übergewichtigen Frauen die Ernährungsumstellung mit einem langfristigen Gewichtsverlust verbunden ist.
Bewegung
Einfluss vor der Krebsdiagnose
Im Gegensatz zu den vorangehenden Themen, wo es um die Unterstützung des Verzichtes geht, kann die Patientin nun wortwörtlich selbst aktiv werden.
Körperliche Aktivität senkt das relative Risiko, an Krebs zu erkranken, für einige Krebsarten deutlich. Es korreliert mit dem Ausmass der Aktivität hinsichtlich Intensität und Dauer und hat den gleichen Effekt auf Übergewichtige wie auch auf normalgewichtige Frauen. Aktive Frauen haben im Vergleich zu kaum aktiven Frauen ein um 13% geringeres Risiko, an Mammakarzinom zu erkranken, bzw. ein um 20% geringeres Risiko, an einem Endometriumkarzinom zu erkranken.
Durch körperliche Aktivität wird die Durchblutung des gesamten Körpers gefördert, steigert sich der Energiehaushalt und wird das Immunsystem gestärkt. Die Spiegel von Insulin, Sexualhormonen und Wachstumsfaktoren, welche das Krebswachstum fördern, werden gesenkt. Sport reduziert den Östrogenspiegel im Blut und Gewebe, was insbesondere bei Frauen mit hormonabhängiger Krebserkrankung relevant ist. Sport steigert den Energiehaushalt, unterstützt das Halten eines gesunden Körpergewichts, reduziert den Körperfettanteil und wirkt sich positiv auf die Psyche aus.
Beratung während der Behandlung und in der Nachsorge
Bewegung und Sport bei onkologischen Erkrankungen ist ein relevantes Thema. In Anbetracht der starken Evidenz und der grossen Nachfrage seitens der Patientinnen wird eine neue S3-Leitlinie zur Bewegungstherapie bei onkologischen Erkrankungen entwickelt. Die Aufrechterhaltung körperlicher Aktivität und regelmässige Trainings sind wesentliche Bestandteile einer modernen multidisziplinären Krebsbehandlung. Mit körperlicher Aktivität zeigen sich eine Prognoseverbesserung und eine Senkung der Mortalität. Körperlich aktive Brustkrebsüberlebende haben gegenüber den am wenigsten Aktiven ein um 40% geringeres Risiko, an Brustkrebs zu sterben. Neben der Verringerung der Mortalität hat körperliche Aktivität weitreichende positive Effekte auf die Lebensqualität. Dazu gehört eine Verbesserung der körperlichen Funktionalität sowie eine Reduktion von Angstgefühlen und Depression. Bewegung ist ein wesentlicher Grundpfeiler in der Prävention und Therapie von krebsspezifischer Fatigue. Onkologische Patientinnen sollen zur körperlichen Aktivität unter und nach Abschluss der onkologischen Therapie motiviert werden. Körperliche Inaktivität gilt es zu vermeiden. Insbesondere wird empfohlen, so früh wie möglich nach der Diagnose mindestens 150 Minuten moderate oder 75 Minuten anstrengende körperliche Aktivität pro Woche zu erreichen und aufrechtzuerhalten. Der Trainingsfokus sollte auf Ausdauer, Kraft, Koordination und Beweglichkeit gesetzt werden.
Literatur:
bei den Verfasserinnen
Das könnte Sie auch interessieren:
Unser Universimed-Team berichtet für Sie aus Salzburg!
Die Jahrestagung der OEGGG findet in diesem Jahr vom 30. Mai bis 2. Juni in Salzburg statt. Diese Veranstaltung ist zweifelsohne eine der bedeutendsten Tagungen für Gynäkologinnen und ...
OeGGG 2018
...
OeGGG 2018
Test...