Parkinsonprävention durch Lebensstilmodifikation
Autor:innen:
Martin Rodemann1,2
Dr. Anja Ophey3
Dr. Ambra Stefani4
Priv.-Doz. Dr. Eva Schäffer5
Priv.-Doz. Dr. Michael Sommerauer1,2
1 Klinik für Parkinson, Schlaf- und Bewegungsstörungen, Zentrum für Neurologie Universitätsklinikum Bonn, Universität Bonn
2 Deutsches Zentrum für neurodegenerative Erkrankungen (DZNE) Bonn
3 Medizinische Psychologie | Neuropsychologie & Gender Studies
Medizinische Fakultät und Universitätsklinikum Köln, Universität zu Köln
4 Zentrum für Schlafmedizin
Universitätsklinik für Neurologie
Medizinische Universität Innsbruck
5 Klinik für Neurologie
Universitätsklinikum Schleswig-Holstein
Campus Kiel
Korrespondierender Autor:
Martin Rodemann
E-Mail: Martin.Rodemann@ukbonn.de
Noch bevor die ersten motorischen Symptome der Parkinsonkrankheit auftreten, beginnt die Erkrankung auf biologischer Ebene. Auch wenn bislang keine pharmakologische Neuroprotektion oder Krankheitsmodifikation möglich ist, eröffnen Lebensstilmodifikationen wie gesteigerte körperliche und geistige Aktivität vielversprechende nichtpharmakologische Ansatzpunkte. Insbesondere Personen mit isolierter REM-Schlaf-Verhaltensstörung könnten von solchen präventiven Strategien profitieren – mit dem Ziel, das Auftreten klinischer Symptome hinauszuzögern und den Verlauf abzumildern.
Keypoints
-
Ein standardisiertes Screening im neurologischen Alltag ist essenziell, um Risikopersonen zu identifizieren und präventive Ansätze zu ermöglichen.
-
Lebensstilmodifikationen könnten als präventive Maßnahme zukünftig in die standardisierte Versorgung von frühen α-Synukleinopathien integriert werden.
-
Angesichts fehlender pharmakologischer Optionen bieten Lebensstilmodifikationen erhebliches gesundheitliches und ökonomisches Potenzial.
-
Vielfältige präventive Maßnahmen stehen bereits heute für Personen im Frühstadium von α-Synukleinopathien zur Verfügung.
Einleitung
Die Parkinsonkrankheit ist eine progressive neurodegenerative Erkrankung, die primär klinisch durch ihre motorischen Symptome (Bradykinesie plus Ruhe-Tremor/Rigor) gemäß den internationalen „Movement Disorder Society“(MDS)-Kriterien definiert wird.1 Den offensichtlichen krankheitsdefinierenden motorischen Symptomen gehen typischerweise subtilere Bewegungsveränderungen und auch häufig nichtmotorische Beschwerden wie Schlafstörungen, kognitive Beeinträchtigungen, Obstipation, Hyposmie und autonome Funktionsstörungen bereits um Jahre voraus. Dieser Zeitraum ist als prodromale Phase der Parkinsonkrankheit anzusehen,2 für welche eigene Kriterien der MDS definiert wurden.3 Biologisch beginnt die Parkinsonkrankheit nochmals deutlich früher: Bereits bis zu Jahrzehnte vor Diagnosestellung finden sich pathologische α-Synuklein-Aggregate in Strukturen des zentralen und peripheren Nervensystems.4,5 Insbesondere die intrazellulären Ablagerungen von α-Synuklein-Aggregaten werden neben weiteren neuronalen Prozessen als pathophysiologisch ursächlich für die progressive Neurodegeneration angesehen.6–8 Pathologisches, fehlgefaltetes α-Synuklein kann heutzutage mittels hochsensitiver Seed-Amplification-Assays (SAA) aus verschiedenen Biomaterialien wie z.B. Liquor (extrazelluläres α-Synuklein) oder Hautbiopsien (intra- und extrazelluläres α-Synuklein) nachgewiesen werden. Hierbei nutzten SAAs die Fähigkeit von fehlgefaltetem α-Synuklein, die Aggregation von normalem α-Synuklein zu induzieren („seeding“).9 Die klinische Relevanz einer isolierten α-Synuklein-Positivität in hochsensitiven Assays (bei fehlender Symptomatik) für das Auftreten einer Parkinsonkrankheit ist derzeit Gegenstand wissenschaftlicher Diskussion.
Rolle von Lebensstilmodifikationen bei der Parkinsonkrankheit
Lebensstilmodifikationen wie körperliche und geistige Aktivität, gesunde Ernährung und Stressmanagement können neben symptomatischen Verbesserungen auch krankheitsmodifizierende Effekte bei bereits bestehender Parkinsonkrankheit erzielen.10 Moderate bis hochintensive aerobe Übungen stabilisieren motorische Symptome nicht nur kurzfristig, sondern auch in Langzeitstudien über mehrere Jahre hinweg. Darüber hinaus haben aber auch schon leichte bis moderate Aktivitäten wie zügiges Gehen einen nachweislich positiven Effekt.11,12 Verschiedene Bewegungsformen wie Tai-Chi, Boxen oder Pilates können aufgrund der gemeinschaftlichen Organisation die Adhärenz der Betroffenen erhöhen und konnten in Studien zudem nichtmotorische Symptome verbessern.13–18 Diätetische Maßnahmen, wie z.B. die mediterrane Diät, zeigen in ersten kleineren Studien ebenfalls positive Effekte auf Kognition und Obstipation, wobei motorische Symptomverbesserungen inkonsistent sind.19,20 Achtsamkeitsbasierte Interventionen konnten signifikant Depression und Angststörungen reduzieren.21 Als Mechanismen, die diesen krankheitsmodifizierenden Effekten zugrunde liegen, werden neuroplastische Veränderungen (u.a. eine erhöhte funktionelle Konnektivität zwischen Basalganglien und Kortex sowie eine reduzierte Hirnatrophie), eine Reduktion von oxidativem Stress und Neuroinflammation sowie möglicherweise auch epigenetische Modulationen diskutiert.22–24 In diesem Sinne erhöhen solche Interventionen die neuronale Resilienz gegenüber der Krankheit.
Prävention
α-Synukleinopathien sind nach der Alzheimerkrankheit die zweithäufigste Gruppe neurodegenerativer Erkrankungen. Es wird ein starker Anstieg ihrer Prävalenz erwartet, sodass bis zum Jahr 2040 weltweit mehr als 12 Millionen Menschen betroffen sein könnten.25 Trotz ihrer hohen Prävalenz stehen bislang keine pharmakologischen krankheitsmodifizierenden Behandlungen für α-Synukleinopathien zur Verfügung, sodass präventive Maßnahmen zunehmend in den Fokus gerückt werden sollten. Auch wenn es sich bei diesen präventiven Maßnahmen im klinischen Kontext zwar um Primärprävention (Abwesenheit von krankheitsspezifischen Symptomen) handelt, muss man im biologischen Kontext jedoch bereits von Sekundärprävention (Nachweis pathophysiologisch ursächlicher α-Synuklein-Aggregate) sprechen. Zum Zeitpunkt der Parkinsondiagnose sind bereits 50–70% aller dopaminergen Neurone der Substantia nigra untergegangen, was biologisch einem fortgeschrittenen Stadium der Neurodegeneration entspricht.26 Um bereits zu einem früheren Zeitpunkt des Krankheitsprogresses anzusetzen, rekrutieren derzeit verschiedene Interventionsstudien in Deutschland und Österreich Betroffene im Frühstadium von α-Synukleinopathien (iRBD oder Early-PD). Ziel ist es, die Effekte von Lebensstilinterventionen – wie kognitivem Training, vermehrter sportlicher Aktivität und multimodalen Maßnahmen – in der Frühphase der Erkrankung zu untersuchen.
Früherkennung
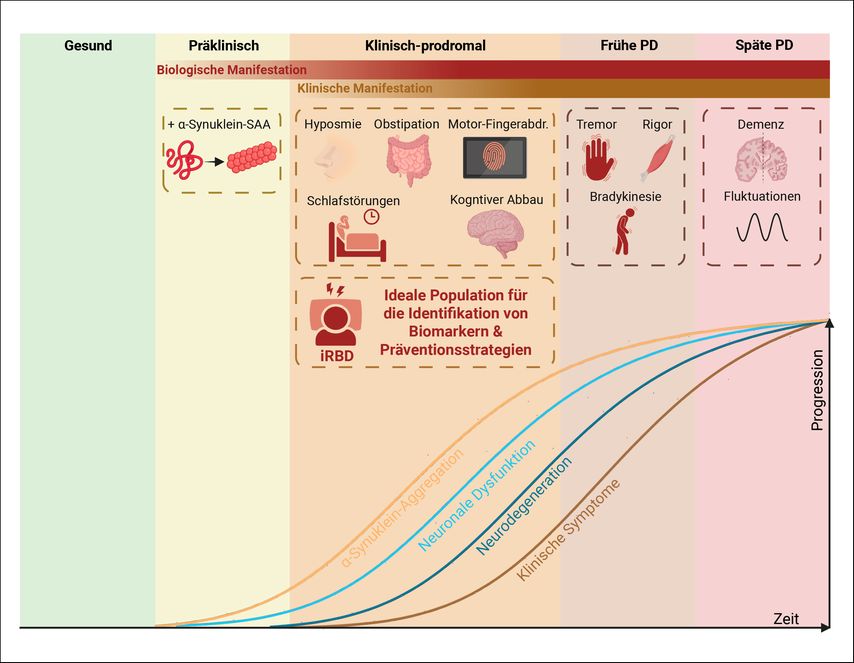
Um Personen mit einem erhöhten Krankheitsrisiko frühzeitig präventive Maßnahmen zukommen lassen zu können, spielt die Früherkennung von entsprechenden Personen eine wesentliche Rolle. Die isolierte REM-Schlaf-Verhaltensstörung (iRBD) ist eine Parasomnie, die durch den Verlust der physiologischen Muskelatonie während des REM-Schlafs und durch Traum-Enactment-Verhalten (z.B. Schlagen, Treten und Schreien) gekennzeichnet ist und mittels Polysomnografie zuverlässig diagnostiziert werden kann.27 Bis zu 90% der Personen mit iRBD entwickeln innerhalb von 20 Jahren nach der Diagnose eine Parkinsonkrankheit, entweder mit reinem motorischem Phänotyp oder auch mit deutlichen kognitiven Einschränkungen – mit einer etwa gleichmäßigen Verteilung zwischen beiden Entitäten.28 In ähnlicher Größenordnung können bereits im Stadium der iRBD α-Synuklein-Aggregate im Liquor oder in Hautbiopsien mittels SAA nachgewiesen werden, sodass die iRBD klinisch ein Prodromalstadium der Parkinsonkrankheit und biologisch eine frühe α-Synukleinopathie darstellt (Abb. 1).29 Als pathophysiologisch ursächlich für den Verlust der REM-Atonie wird die Ablagerung von α-Synuklein-Aggregaten im Locus subcoeruleus angenommen, ohne dass zu diesem Zeitpunkt weiter rostral liegende motorische Zentren wie die Substantia nigra relevant betroffen sind.30 Personen mit einer iRBD stellen daher neben der Identifikation von Früherkennungs-Biomarkern eine besonders geeignete Zielgruppe zur wissenschaftlichen Untersuchung von Lebensstilinterventionen dar.28 Ziel ist es, solche Interventionen zu identifizieren, die das Fortschreiten der Erkrankung in einem frühen Stadium verlangsamen können. Die International RBD Study Group ( https://irbdsg.com ) widmet sich seit vielen Jahren der systematischen Erforschung dieser Erkrankung. An mehreren Zentren weltweit werden mittlerweile große iRBD-Kohorten systematisch betreut – alleine in Bonn unter Leitung von Michael Sommerauer zum Beispiel über 150 Personen. Die prospektive neurologische Begleitung dieser Kohorten bietet insbesondere im Kontext präventiver Strategien einen substanziellen klinischen Nutzen für die Betroffenen.
Abb. 1: Progression der Parkinsonkrankheit (biologisch vs. klinisch). Abkürzungen: SAA, „Seed Aggregation Assay“; PD, Parkinsonkrankheit; Motor-Fingerabdr., digitale Detektion frühester motorischer Veränderungen. Created in BioRender. Sommerauer, M. (2026) https://BioRender.com/pdx6fqf
CogTrAiL-RBD-Studie – kognitives Training & gesunder Lebensstil
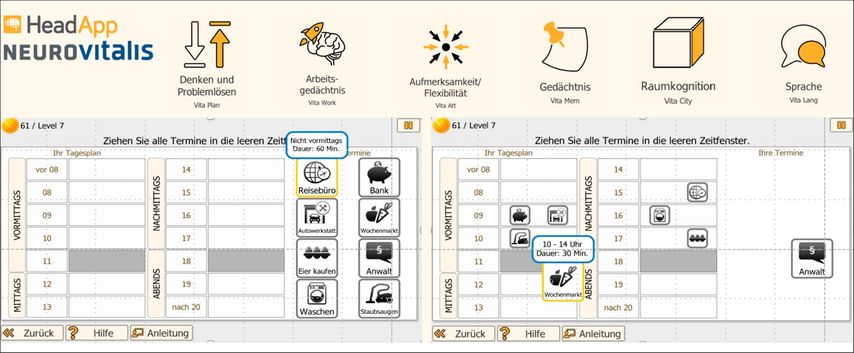
Neben der progredienten motorischen Verschlechterung ist der kognitive Abbau ein Schlüsselelement des nichtmotorischen Symptomkomplexes von α-Synukleinopathien. Die CogTrAiL-RBD-Studie ( https://drks.de/search/de/trial/DRKS00024898 ) untersucht als randomisierte, kontrollierte, einfach verblindete 2-Phasen-Studie die Wirksamkeit und Machbarkeit einer kognitiven Intervention bei 82 Personen mit polysomnografisch bestätigter iRBD.31 In der ersten Phase erhält eine Early-Start-Gruppe (n=40) ein digitales, kognitives Training via Tablet/Smartphone-App oder am Computer (HeadApp/NEUROvitalis, HelferApp GmbH) mit adaptiven Einheiten, die flexibel von zu Hause aus absolviert werden können (15 Tage à 40 Minuten über 5 Wochen; Abb. 2), ergänzt durch Psychoedukation zu einem gesunden, aktiven Lebensstil. Eine Delayed-Start-Gruppe (n=42) erhält zunächst noch keine Intervention und fungiert als Kontrollgruppe. In der zweiten Phase erhalten beide Gruppen die beschriebene Intervention. Pro Phase finden je zwei klinische Visiten statt (direkt nach dem Training und nach 6 Monaten). Eine gesunde, alters- und geschlechtsgematchte Kontrollgruppe (n=50) dient dem Vergleich. Primärer Endpunkt sind Veränderungen der Exekutivfunktionen. Sekundäre Endpunkte sind Veränderungen der globalen Kognition, anderer kognitiver Domänen, der Lebensqualität, motorischer/nichtmotorischer Symptome, des Schlafverhaltens (Polysomnografie) sowie struktureller und funktioneller MRT-Bildgebung. Die Studie wird unter Leitung der Universität Köln (Anja Ophey und Elke Kalbe) in Kooperation mit der Universität Bonn (Michael Sommerauer) durchgeführt. Die Rekrutierung läuft seit Juni 2022; die Studie steht kurz vor dem Abschluss und voraussichtlich im April 2026 werden alle Teilnehmenden die aktive Studienphase durchlaufen haben. Vorläufige Daten für die erste Studienphase zeigen bereits eine signifikante Verbesserung der Exekutivfunktionen, was auch im längerfristigen Verlauf nach 6 Monaten noch nachweisbar ist. Weitere Ergebnisse werden auf der diesjährigen AD/PD-Konferenz in Kopenhagen präsentiert werden.
Abb. 2: Digitales, kognitives Training via Tablet/Smartphone-App oder am Computer (HeadApp/NEUROvitalis, HelferApp GmbH)
ALPHA-FIT-Studie – körperliches Training
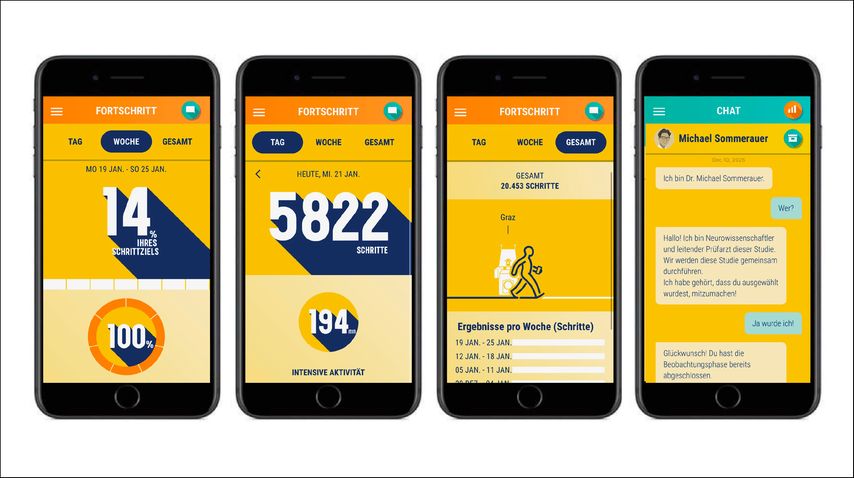
Eine Steigerung der körperlichen Aktivität könnte dazu beitragen, neurodegenerative Prozesse im Frühstadium von α-Synukleinopathien zu verlangsamen. Studien aus Tiermodellen und klinische Untersuchungen weisen darauf hin, dass regelmäßige körperliche Aktivität krankheitsmodifizierende Effekte haben und insbesondere kognitive Funktionen erhalten kann.32,33 Jedoch erreichen viele Personen nicht das von der WHO empfohlene allgemeine Bewegungsniveau.34 Aktuell gewinnen digitale, motivierende Smartphone-Apps an Bedeutung, da sie eine einfache und skalierbare Möglichkeit bieten, körperliche Aktivität im Alltag zu fördern.35 Ziel der ALPHA-FIT-Studie36 ( https://www.dzne.de/forschung/studien/klinische-studien/alpha-fit ) ist es, die Effekte einer gesteigerten körperlichen Aktivität im Alltag auf die kognitiven Funktionen bei Personen mit iRBD und gesunden Kontrollen zu untersuchen. In der randomisierten, doppelblinden und aktiv kontrollierten Studie werden die Teilnehmenden über einen Zeitraum von einem Jahr zur Steigerung der körperlichen Aktivität motiviert. Alle Teilnehmenden erhalten hierzu Zugang zu einer motivationsfördernden Smartphone-App mit Gamification-Elementen (ALPHA-FIT-App, Abb.3), dessen Grundstruktur im Rahmen der Slow-SPEED-Studie37 entwickelt wurde. Die App ist zur kontinuierlichen Aufzeichnung der körperlichen Aktivität (Schrittzahl/Herzfrequenz) mit einer Fitbit-Smartwatch verbunden. Nach einer 4-wöchigen Beobachtungsphase zur Erfassung der Ausgangsaktivität erfolgt die Randomisierung in eine Interventionsgruppe (100%ige Steigerung der körperlichen Aktivität) oder eine aktive Kontrollgruppe (10%ige Steigerung). Über die App können individuell angepasste, zielgerichtete Motivationsmaßnahmen vermittelt sowie die Erreichung der Aktivitätsziele unmittelbar überprüft werden. Primärer Outcome-Parameter ist die Veränderung der kognitiven Leistung über ein Jahr. Neben klassischen neuropsychologischen Tests als primärem Endpunkt werden als sekundäre Endpunkte MRT- und blutbasierte Marker der Hirnalterung untersucht. Die Studie – als Spin-off der Slow-SPEED-Studie37 – wird unter Leitung der Universität Bonn (Michael Sommerauer) in enger Kooperation mit der Radboud-Universität (Sirwan Darweesh) und der Medizinischen Universität Innsbruck (Ambra Stefani) durchgeführt. Insgesamt ist ein gemeinsamer Einschluss von über 250 Personen mit iRBD und 100 alters- und geschlechtsgematchten Kontrollen geplant; die Rekrutierung ist 12/2025 gestartet.
Prevention-in-PD – multimodale Lebensstilintervention bei (prodromaler) Parkinsonkrankheit
Eine Kombination aus multiplen – sich ergänzenden – Interventionen könnte die Effekte nichtpharmakologischer Therapien nochmals steigern.38 Eine zentrale klinische Herausforderung besteht jedoch darin, dass Betroffene häufig Schwierigkeiten haben, mehrere Verhaltensinterventionen gleichzeitig umzusetzen. Die Prevention-in-PD-Studie39 ( https://prevention-in-pd.de ) ist eine klinische Machbarkeitsstudie, die untersucht, ob ein multimodales Lebensstilprogramm die Adhärenz gegenüber empfohlenen Verhaltensänderungen bei Personen mit Parkinsonkrankheit und Personen mit iRBD verbessern kann. Das sechsmonatige Interventionsprogramm umfasst vier integrierte Säulen: strukturiertes körperliches Training, Ernährungsberatung mit Fokus auf mediterrane Ernährung, Schlafcoaching und digitales kognitives Training. Das Programm wird durch psychoedukative Maßnahmen, fertigkeitsorientiertes Training und individuelle Personalisierung ergänzt, um praktische Anwendbarkeit und Motivationserhalt zu sichern. Die primäre Forschungsfrage zielt darauf ab, ob Teilnehmende mit manifester Parkinsonkrankheit (n=66) oder iRBD (n=33) in der Lage sind, ein kombiniertes Lebensstilprogramm über einen Zeitraum von sechs Monaten konsistent umzusetzen. Sekundär werden potenzielle frühe Effekte auf symptomatische Parameter, Lebensqualität und allgemeine Gesundheitsindikatoren erfasst. Die Studie wird unter Leitung der Universität Kiel (Eva Schäffer und Daniela Berg) in Kooperation mit der Universität Lübeck (Norbert Brüggemann), der Universität Köln (Anja Ophey und Elke Kalbe), der Universität Marburg (David Pedrosa) und der Universität Bonn (Michael Sommerauer) durchgeführt; die Rekrutierung ist ab 4/2026 geplant.
Fazit
Die Ergebnisse der exemplarisch erwähnten Interventionsstudien (CogTrAiL-RBD, ALPHA-FIT und Prevention-in-PD) in der D-A-CH-Region könnten bei positivem Ausgang einen Wendepunkt für die Integration von Lebensstilmodifikationen in die standardisierte Versorgung von frühen α-Synukleinopathien im deutschsprachigen Raum und auch international darstellen. Dies könnte den Grundstein für einen präventiven Behandlungsansatz insbesondere bei der iRBD legen, was gerade im Hinblick auf die noch fehlenden pharmakologischen Therapiemöglichkeiten ein enormes gesundheitliches und ökonomisches Potenzial bietet.
Begleitend müssen jedoch auch standardisierte Maßnahmen zur Früherkennung Einzug in den klinischen Alltag in der Neurologie erhalten. Nur durch ein breites Screening können ein relevanter Anteil der Risikogruppe identifiziert werden und eine Verlangsamung der neurodegenerativen Prozesse erreicht werden. Die verlässliche Identifikation frühester (nicht-)motorischer Symptome hängt maßgeblich von der Sensitivität und Spezifität der verfügbaren Screening-Instrumente ab. Eine weitere Optimierung dieser Verfahren könnte künftig eine noch frühere Detektion entsprechender klinischer Symptome ermöglichen und somit die zeitlich-diagnostische Lücke zur biologisch definierten α-Synuklein-Positivität schließen. Bezüglich der Nomenklatur ist zu beachten, dass „α-Synukleinopathie“ ein biologisch und kein klinisch geprägter Begriff ist: Das Prodromalstadium primär klinisch definierter Krankheiten wie der Parkinsonkrankheit oder Lewy-Körper-Demenz enstpricht daher bereits einer frühen (und nicht prodromalen) α-Synukleinopathie.
Nach erfolgreicher Identifikation der Risikogruppe stehen bereits heute außerhalb von Studien vielfältige präventive Maßnahmen für Personen im Frühstadium von α-Synukleinopathien zur Verfügung. Hierzu zählen die häufig in Smartphone-Betriebssystemen integrierten Gesundheits-Apps (z.B. Health, Google Fit), die Bewegungsdaten erfassen und durch motivierende Elemente die körperliche Aktivität fördern. Dies kann durch Verordnung der als digitale Gesundheitsanwendung (DiGA) zugelassenen App NeuroNation MED für personalisiertes kognitives Training ergänzt werden. Begleitend empfiehlt sich eine Beratung zu einem gesunden, aktiven Lebensstil.
Literatur:
1 Postuma RB et al.: MDS clinical diagnostic criteria for Parkinson’s disease. Mov Disord 2015; 30(12): 1591-601 2 Bloem BR et al.: Parkinson’s disease. Lancet 2021; 397(10291): 2284-303 3 Heinzel S et al.: Update of the MDS research criteria for prodromal Parkinson’s disease. Mov Disord 2019; 34(10): 1464-70 4 Braak H et al.: Staging of brain pathology related to sporadic Parkinson’s disease. Neurobiol Aging 2003; 24(2): 197-211 5 Ferrer I et al.: Neuropathology of sporadic Parkinson disease before the appearance of parkinsonism: preclinical Parkinson disease. J Neural Transm (Vienna) 2011; 118(5): 821-39 6 Simuni T et al.: A biological definition of neuronal α-synuclein disease: towards an integrated staging system for research. Lancet Neurol 2024; 23(2): 178-90 7 Reyes NGD et al.: Revisiting Parkinson’s disease definition and classification: insights from two emerging biological frameworks. J Neural Transm (Vienna) 2025; https://doi.org/10.1007/s00702-025-03013-y (2025) doi:10.1007/s00702-025-03013-y 8 Morrisx HR et al.: The pathogenesis of Parkinson’s disease. Lancet 2024; 403(10423): 293-304 9 Bellomo G et al.: α-Synuclein seed amplification assays for diagnosing synucleinopathies: The way forward. Neurology 2022; 99(5): 195-205 10 Trinh J et al.: The role of lifestyle interventions in symptom management and disease modification in Parkinson’s disease. Lancet Neurol 2026; 25(1): 90-102 11 Cancela JM et al.: Effects of a high-intensity progressive-cycle program on quality of life and motor symptomatology in a Parkinson’s disease population: A pilot randomized controlled trial. Rejuvenation Res 2020; 23(6): 508-15 12 Linder SM et al.: An 8-week aerobic cycling intervention elicits improved gait velocity and biome-chanics in persons with Parkinson’s disease. Gait Posture 2022; 98: 313-5 13 Li G et al.: Tai Chi improves non-motor symptoms of Parkinson’s disease: One-year randomized con-trolled study with the investigation of mechanisms. Parkinsonism Relat Disord 2024; 120: 105978 14 Chang CL et al.: Distinct effects of long-term Tai Chi Chuan and aerobic exercise interventions on motor and neurocognitive performance in early-stage Parkinson’s disease: a randomized controlled trial. Eur J Phys Rehabil Med 2024; 60(4): 621-33 15 Sangarapillai K et al.: Boxing vs sensory exercise for Parkinson’s disease: A double-blinded randomized controlled trial. Neurorehabil Neural Repair 2021; 35(9): 769-77 16 Patel RA et al.: A pilot study of a 12-week community-based boxing program for Parkinson’s disease. J Clin Neurosci 2023; 107: 64-7 17 de Faria J et al.: Multicomponent and mat Pilates training increased gait speed in individuals with Parkinson’s disease when walking and carrying a load: A single-blinded randomized controlled trial. Physiother Res Int 2023; 28(4): e2031 18 Çoban F et al.: Effect of clinical Pilates training on balance and postural con-trol in patients with Parkinson’s disease: a randomized controlled trial. J Comp Eff Res 2021; 10(18): 1373-83 19 Paknahad Z et al.: The effect of the Mediterranean diet on cognitive function in patients with Parkinson’s disease: A randomized clinical controlled trial. Complement Ther Med 2020; 50: 102366 20 Rusch C et al.: Promotion of a mediterranean diet alters constipation symptoms and fecal calprotectin in people with Parkinson’s disease: A randomized controlled trial. Nutrients 2024; 16(17): 2946 21 Yi M et al.: The effects of mindfulness-based interventions in people with Parkinson’s disease: A systematic review and meta-analysis. Clin Gerontol 2025; 48(4): 570-88 22 Johansson ME et al.: Aerobic exercise alters brain function and Structure in Parkinson’s disease: A randomized controlled trial. Ann Neurol 2022; 91(2): 203-16 23 Tari AR et al.: Neuroprotective mechanisms of exercise and the importance of fitness for healthy brain ageing. Lancet 2025; 405(10484): 1093-118 24 Tang X et al.: Epigenetic clock acceleration is linked to age at onset of Parkinson’s disease. Mov Disord 2022; 37(9): 1831-40 25 GBD 2016 Parkinson’s Disease Collaborators: Global, regional, and national burden of Parkinson’s disease, 1990-2016: A systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol 2018; 17(11): 939-53 26 Fearnley JM, Lees AJ: Ageing and Parkinson’s disease: substantia nigra regional selectivity. Brain 1991; 114( Pt 5): 2283-301 27 Boeve BF et al.: Pathophysiology of REM sleep behaviour disorder and relevance to neurodegenerative disease. Brain 2007; 130(Pt 11): 2770-88 28 Postuma RB et al.: Risk and predictors of dementia and parkinsonism in idiopathic REM sleep behaviour disorder: a multicentre study. Brain 2019; 142(3): 744-59 29 Iftikhar IH et al.: Alpha-synuclein pathology in isolated rapid eye movement sleep behaviour disorder: a meta-analysis. J Sleep Res 2024; 33(6): e14204 30 Knudsen K et al.: In-vivo staging of pathology in REM sleep behaviour disorder: a multimodality ima-ging case-control study. Lancet Neurol 2018; 17(7): 618-28 31 Ophey A et al.: Cognitive training and promoting a healthy lifestyle for individuals with isolated REM sleep behavior disorder: study protocol of the delayed-start randomized controlled trial CogTrAiL-RBD. Trials 2024; 25(1): 428 (2024) 32 Petzinger GM et al.: Exercise-enhanced neuroplasticity targeting motor and cognitive circuitry in Parkinson’s disease. Lancet Neurol 2013; 12(7): 716-26 33 Diaz-Galvan P et al.: Association of physical exercise with structural brain changes and cognitive decline in patients with early Parkinson disease. Neurology 2025; 105(5): e213932 34 van Nimwegen M et al.: Physical inactivity in Parkinson’s disease. J Neurol 2011; 258(12): 2214-21 35 Schootemeijer S et al.: Promoting physical activity in people with Parkinson’s disease through a smartphone app: A Pilot Study. J Neurol Phys Ther 2025; 49(2): 74-81 36 Sommerauer DM: Slowing cognitive decline in alpha-synucleinopathies by enhancing physical activity. 2026; https://clinicaltrials.gov/study/NCT07324330 37 Study Details | NCT06193252 | Slow-SPEED-NL: Slowing Parkinson’s early through exercise dosage-Netherlands | ClinicalTrials.gov. https://clinicaltrials.gov/study/NCT06193252 38 Ngandu T et al.: A 2 year multidomain intervention of diet, exercise, cognitive training, and vascular risk monitoring versus control to prevent cognitive decline in at-risk elderly people (FINGER): a randomised controlled trial. Lancet 2015; 385(9984): 2255-63 39 Study Details | NCT07297407 | Prevention-in-PD-Study | ClinicalTrials.gov. https://clinicaltrials.gov/study/NCT07297407
Das könnte Sie auch interessieren:
Lichtblicke für die Therapie von Muskelerkrankungen
Die Tagung „UpDate Muskelforschung“ fand 2026 bereits zum 14. Mal statt. Trotz der Seltenheit der Muskelerkrankungen gab es in den letzten Jahren einige Fortschritte. Neben den aktuell ...
Neuroonkologie: neue therapeutische Möglichkeiten
Lange musste in der Neuroonkologie auf eine Medikamenten-zulassung gewartet werden. Dank intensiver Forschung mit detaillierter molekularer Tumorcharakterisierung konnte im letzten Jahr ...
Palliativmedizin und Neurologie zusammen denken
Viele neurologische Erkrankungen sind chronisch-progredient, mit hoher Symptomlast und begrenzter Heilungsperspektive – und doch wird Palliative Care in der Neurologie oft erst spät oder ...