Modulateurs du récepteur de la sphingosine-1-phosphate dans le traitement de la SEP
Compte-rendu:
Felix Schmidtner, MSc
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les modulateurs du récepteur de la sphingosine-1-phosphate représentent une classe de médicaments prometteurs pour le traitement de deuxième ligne de la sclérose en plaques (SEP). Deux études récentes ont comparé les affinités de liaison et les profils de sécurité de ces médicaments modificateurs de la maladie.
Les sphingosines sont une classe de lipides présents dans tout le corps. Elles sont particulièrement fréquentes dans le cerveau, et elles constituent la structure de base de la sphingomyéline, dont sont composées les gaines de myéline. Les phosphates de sphingosine se lient en outre aux récepteurs de la sphingosine-1-phosphate (S1P) des cellules T. Les modulateurs de récepteurs S1P peuvent ainsi lier les cellules T dans les ganglions lymphatiques et réduire le nombre de cellules T autoréactives dans le cas de la SEP.
Différentes affinités d’attachement déterminantes
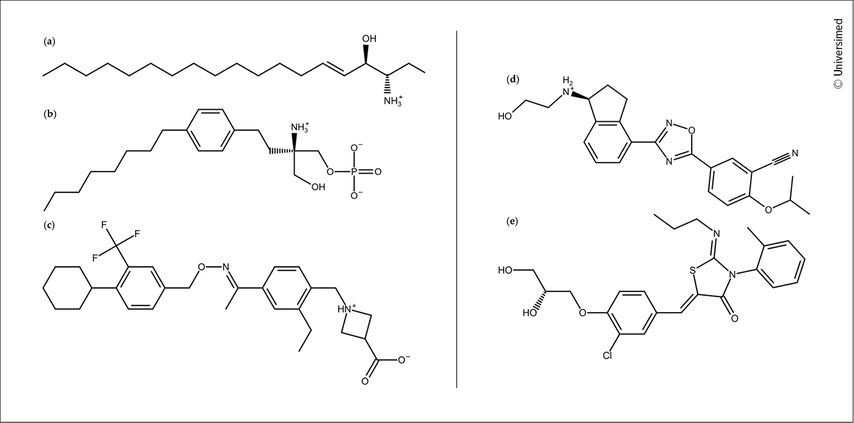
Kores et al. 2024 ont analysé les affinités de liaison des quatre modulateurs de récepteurs S1P autorisés dans l’UE dans le cadre de simulations moléculaires. Même si les quatre modulateurs sont des composés de faible poids moléculaire, leur structure chimique est très différente. Si le premier principe actif autorisé, le fingolimod, est encore celui qui ressemble le plus à la sphingosine avec son résidu d’acide phosphorique, les autres modulateurs ont un aspect nettement différent (Fig.1).1
Fig.1: Structures chimiques du phosphate de sphingosine-1 naturel (a) et des modulateurs de récepteurs S1P utilisés pour le traitement de la sclérose en plaques. b: Fingolomid, c: Siponimod, d: Ozanimod, e: Ponésimod1
Les auteurs se sont concentrés sur les mutations du gène de récepteurs S1P présentes dans la population, appelées «single nucleotide polymorphisms» (SNP), et ont simulé leur influence sur le comportement de liaison des modulateurs vis-à-vis du récepteur. Ces SNP ont tous entraîné une modification de l’affinité de liaison. La S1P naturelle se lie le mieux lorsqu’aucun des SNP n’est présent dans le récepteur. Les modulateurs ont toutefois montré une plus grande affinité de liaison lorsqu’au moins un SNP était présent dans le gène récepteur. Le siponimod se lie le mieux pour toutes les variantes de gènes étudiées. Cependant, l’ozanimod et le ponésimod présentent également un meilleur comportement de liaison que le récepteur de type sauvage, quelle que soit la variante génétique. Le fingolimod a fait preuve d’une meilleure affinité de liaison pour trois variantes de gènes. Il convient de noter qu’il s’agissait de variantes génétiques rares et que l’efficacité d’un médicament ne dépend pas uniquement de l’affinité de liaison, mais également d’autres facteurs tels que la pharmacocinétique et la tolérance.
Sur la base de ces résultats, les auteurs recommandent les substances suivantes pour les différentes mutations:
-
en cas de mutation M1243.32T ou V1323.40M: ozanimod
-
en cas de mutation F2055.42L: siponimod (alternative: ozanimod ou ponésimod)
-
en cas de mutation T2075.44I: siponimod ou ponésimod
-
en cas de mutation T2115.48P: fingolimod
-
pour A2937.35T ou A2937.35V: siponimod, ponésimod ou fingolimod (alternative: ozanimod)
Efficacité des modulateurs du récepteur de la sphingosine-1-phosphate
Un article publié en 2024 par Coyle et al. donne un aperçu de l’efficacité et de la tolérance des quatre modulateurs de récepteurs S1P présentés précédemment. L’objectif était de mettre en évidence les points communs et les différences entre les substances, qui pourraient jouer un rôle dans l’utilisation pratique chez les patient·es individuel·les.2
Tous les modulateurs de récepteurs S1P ont montré une efficacité comparable dans les études pivots et ont réduit le taux de rechute annuel (ARR) par rapport au placebo. Lors de l’utilisation du fingolimod, de l’ozanimod et du ponésimod, l’ARR était également plus faible par rapport à l’utilisation de l’immunosuppresseur tériflunomide.
Il n’existe pas encore d’études comparant le profil d’efficacité des différents modulateurs de récepteurs SP1 autorisés.
Tolérance et profil d’effets secondaires
Comme décrit précédemment, ces modulateurs se distinguent par leur affinité de liaison avec les différentes sous-classes de récepteurs et par leur demi-vie. Le récepteur est exprimé dans différents organes, ce qui entraîne différents profils d’effets secondaires et nécessite un suivi précis des patient·es. On soulignera en particulier les effets secondaires cardiovasculaires, la lymphopénie et une tendance aux infections graves.
Les quatre modulateurs de récepteurs modulent le rythme cardiaque et peuvent entraîner une bradycardie: le fingolimod avec une réduction de 8–10bpm, le ponésimod de 6bpm, le siponimod de 5–6bpm et l’ozanimod de 1,2bpm. En outre, les quatre substances actives peuvent également provoquer une hypertension. L’effet est le plus fort avec le fingolimod et le plus faible avec l’ozanimod. En raison de ce profil d’effets secondaires, un monitoring cardiologique avec ECG et mesure de la pression artérielle est recommandé, en particulier lors de l’initiation du fingolimod, du ponésimod et du siponimod.
Tous les modulateurs de récepteurs S1P autorisés jusqu’à présent réduisent le nombre de lymphocytes dans le sang, ce qui peut augmenter la tendance aux infections. Cette réduction du nombre de lymphocytes allait de 57% avec l’ozanomide (∼760 cellules/μl) à 70% avec le fingolimod (∼500 cellules/μl), le siponimod (∼560 cellules/μl) et le ponésimod (∼650 cellules/μl). L’utilisation des modulateurs s’est accompagnée dans tous les cas d’une augmentation du risque d’infections, notamment d’infections respiratoires des voies respiratoires supérieures et d’infections herpétiques. Les pneumonies étaient plus fréquentes sous fingolimod et les infections fongiques sous siponimod. Lors de l’initiation, il convient donc de garder un œil sur les infections qui surviennent et de surveiller les niveaux de lymphocytes.
Il faut également tenir compte de l’augmentation potentielle du risque de développer une tumeur. Des carcinomes basocellulaires ont été observés dans toutes les études pivots, avec un faible pourcentage: 2% sous fingolimod vs 1% sous placebo, 0,4% sous ponésimod vs 0,2% sous tériflunomide), 1,1% sous siponimod, aucun pourcentage précis n’a été donné pour l’ozanimod. En outre, des cas isolés de lymphomes ont été rapportés après la mise sur le marché du fingolimod.
Tous les modulateurs de récepteurs S1P ont un effet négatif dépendant de la dose sur la fonction pulmonaire lors de l’initiation. En règle générale, aucun suivi pneumologique de routine n’est nécessaire, car la fonction pulmonaire redevient normale après 1 à 3mois.
En ce qui concerne la fonction hépatique, des valeurs élevées d’alanine et d’aspartate transaminases ont été observées. Avec l’ozanimod et le ponésimod, les valeurs se sont normalisées en 2 à 4semaines, alors qu’avec le fingolimod et le siponimod, elles ne se sont normalisées qu’1 à 2mois après la fin du traitement. En résumé, les effets secondaires les plus fréquents avec les modulateurs de récepteurs S1P sont les infections respiratoires, les maux de tête, l’hypertension, la lymphopénie et les inflammations du nez et de la gorge.
Les modulateurs de récepteurs S1P ne doivent pas être utilisés pendant la grossesse ou en cas de désir d’enfant. Bien qu’aucune étude sur la grossesse n’ait été réalisée, les données précliniques indiquent un risque potentiel pour l’enfant en cas d’utilisation. Les grossesses survenues lors de l’étude pivot sur le fingolimod et qui n’étaient pas connues à l’inclusion dans l’étude ont révélé une exposition in utero. Des malformations ont été observées dans 6% des grossesses. En outre, l’utilisation du fingolimod, de l’ozanimod, du ponésimod et du siponimod a entraîné des avortements.
À quoi faut-il faire attention dans le travail quotidien?
Les professionnels de la santé doivent connaître les effets cardiaques possibles des modulateurs de récepteurs S1P. La prudence est ici de mise en cas d’administration simultanée de bêtabloquants, de digoxine, de bloqueurs des canaux Ca2+ et de traitements allongeant l’intervalle QT en raison des effets cardiovasculaires.
Les directives cliniques d’initiation pour le titrage doivent être respectées.
Pendant l’utilisation des modulateurs de récepteurs S1P, il convient de renoncer aux vaccins vivants atténués. Les éventuelles vaccinations prévues avec des vaccins vivants devraient idéalement être rattrapées avant l’utilisation des modulateurs de récepteurs S1P. La vaccination complète contre le varicelle-zona est également recommandée avant l’utilisation de modulateurs de récepteurs S1P.
Les patient·es doivent être informé·es du risque de leucoencéphalopathie multifocale progressive (LEMP). Celle-ci peut se développer par réactivation du virus John Cunningham, très répandu chez les personnes immunodéprimées, et a été observée principalement lors du traitement par le fingolimod (cas observés lors d’études pivots ou d’extension en ouvert): 64 sous fingolimod, 3 sous siponimod, 1 sous Ozanimod (post-homologation), 0 cas connu sous ponésimod).
En outre, lors de l’utilisation du fingolimod, les patient·es doivent être informé·es que l’arrêt du traitement peut s’accompagner de rechutes graves, parfois invalidantes. Lors de l’utilisation du ponésimod, du siponimod ou de l’ozanimod, de telles rechutes n’ont pas été observées après le sevrage.
Examens recommandés avant l’utilisation
-
Compte tenu des effets cardiovasculaires des modulateurs de récepteurs S1P, un ECG doit être réalisé au préalable. Pour tous/toutes les patient·es ayant des antécédents de problèmes cardiaques tels qu’un allongement de l’intervalle QT, une arythmie, une ischémie ou un infarctus du myocarde, il convient de consulter un·e cardiologue avant d’utiliser le produit.
-
Une analyse de sang doit être effectuée afin de déterminer les taux de cellules sanguines ainsi que de transaminases et de bilirubine.
-
Une évaluation ophtalmologique avant l’utilisation est recommandée pour pratiquement tous les modulateurs. Pour l’ozanimod, elle n’est nécessaire que pour les patient·es à haut risque.
-
Avant d’utiliser le siponimod, le génotype CYP2C9 doit être déterminé.
-
Un examen dermatologique est recommandé pour tous/toutes les patient·es avant de commencer le traitement au siponimod.
Suivi continu
Lors du suivi, l’accent doit être mis sur la tension artérielle, l’ophtalmologie, l’hémogramme (notamment les globules blancs, les lymphocytes, le taux d’aminotransférase hépatique), les altérations cutanées et les éventuelles infections graves. Il convient également de procéder à un contrôle annuel du cancer de la peau. Une évaluation ophtalmologique continue est particulièrement recommandée pour tous/toutes les patient·es ayant des antécédents d’œdème maculaire ou d’uvéite, ainsi que pour les patient·es diabétiques. Si le traitement est arrêté, il faut poursuivre le suivi au moins jusqu’à ce que le taux de lymphocytes soit normalisé.
Contre-indications et interactions
-
Le fingolimod est contre-indiqué chez les patient·es dont l’intervalle QT de base est ≤500msec, ainsi qu’en cas d’arythmie nécessitant des médicaments anti-arythmiques de classe Ia ou III.
-
L’ozanimod est contre-indiqué chez les patient·es présentant un bloc sino-articulaire et en cas d’apnée du sommeil non traitée, et n’est pas recommandé en cas d’utilisation d’inhibiteurs de la MAO; selon l’autorisation suisse, les inhibiteurs de la MAO ne constituent toutefois pas une contre-indication.
-
Le siponimod est contre-indiqué chez les patient·es présentant un génotype CYP2C9*3/*3.
-
La coadministration d’ozanimod avec des opioïdes, des ISRS, des IRSN, des antidépresseurs tricycliques et des tyramines n’est pas recommandée. Toutefois, selon l’autorisation suisse, cela ne constitue pas une contre-indication.
-
Le ponésimod n’est pas recommandé en association avec des inducteurs puissants du CYP3A4 et de l’UGT1A1 (p. ex.: rifampine, phénytoïne, carmazépine).
-
Le siponimod ne doit pas être utilisé en association avec le modafinil et tout type d’inhibiteur ou d’inducteur du CYP2C9 et du CYP3A4.
Leucoencéphalopathie multifocale progressive (LEMP)
Si une LEMP se produit, il convient d’arrêter le traitement par un modulateur de récepteurs S1P.
Les premiers signes de la LEMP sont des symptômes tels que des troubles de la parole et une démence. Un diagnostic différentiel avec détection par PCR du virus dans le LCR combiné à une IRM est possible, mais difficile. De nombreux/nombreuses patient·es sain·es sont également infecté·es et l’image obtenue par IRM ressemble aux foyers de démyélinisation de la SEP.
Si le soupçon persiste, il faut recourir à une autre classe de médicaments pour traiter la SEP. En général, la LEMP est une maladie rare qui touche principalement les patient·es atteint·es de lymphopénie modérée à sévère et les patient·es âgé·es.
L’apparition d’un syndrome de reconstitution immunitaire (IRIS) a également été rapportée chez les patient·es atteint·es de LEMP. En général, celui-ci s’est développé dans les mois qui ont suivi l’arrêt du traitement par les modulateurs de récepteurs S1P.
Syndrome d’encéphalopathie réversible postérieure (PRES)
Un petit nombre de cas de PRES ont également été observés lors de l’administration de fingolimod. Les symptômes comprennent des maux de tête, des troubles visuels, de la confusion et des crises d’épilepsie. Si le PRES n’est pas traité à temps, il peut entraîner des accidents vasculaires cérébraux ischémiques et des hémorragies cérébrales.
Littérature:
1 Coyle PK et al.: Sphingosine 1-phosphate receptor modulators in multiple sclerosis treatment: a practical review. Ann Clin Transl Neurol 2024; 11(4): 842-855 2 Kores K et al.: Computational analysis of S1PR1 SNPs reveals drug binding modes relevant to multiple sclerosis treatment. Pharmaceutics 2024; 16(11): 1413
Das könnte Sie auch interessieren:
Présentation des données pertinentes pour la pratique sur le mavacamten dans la CMHO
Le mavacamten, un inhibiteur de la myosine, a été la première substance de cette classe à être autorisée en 2023 pour le traitement de la cardiomyopathie hypertrophique obstructive (CMHO ...
La perte de poids reste toujours le meilleur traitement en cas de MASLD
La directive commune pour la prise en charge de la maladie stéatosique du foie associée à une dysfonction métabolique (MASLD) de l’European Association for the Study of the Liver (EASL ...
Hypertension secondaire: formes, diagnostic & options thérapeutiques
La fréquence d’une cause secondaire d’hypertension artérielle est de 10%. En cas de suspicion d’hypertension secondaire, il convient de procéder à un examen ciblé afin de pouvoir, dans l ...